0 20309 20317 20323 20327 20333 20335 20339 20345 20347 20353 20359 20363 20365 20369 20375 20377 20383 20387 20389 20393 20395 20399 20401 20403 20404 20405 20407 20408 20409 20411 20413 20417 20419 20423 20425 20429 20435 20437 20443 20447 20449 20453 20459 20465 20467 20473 20477 20479 20485 20489 20495 20503 203614
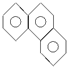 ,其一氯代物的数目为( )
,其一氯代物的数目为( )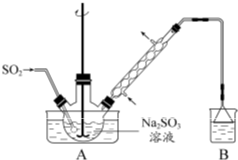 (2012?江苏)[实验化学]次硫酸氢钠甲醛(NaHSO2?HCHO?2H2O)在印染、医药以及原子能工业中应用广泛.以Na2SO3、SO2、HCHO 和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如下:
(2012?江苏)[实验化学]次硫酸氢钠甲醛(NaHSO2?HCHO?2H2O)在印染、医药以及原子能工业中应用广泛.以Na2SO3、SO2、HCHO 和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如下: