0 20197 20205 20211 20215 20221 20223 20227 20233 20235 20241 20247 20251 20253 20257 20263 20265 20271 20275 20277 20281 20283 20287 20289 20291 20292 20293 20295 20296 20297 20299 20301 20305 20307 20311 20313 20317 20323 20325 20331 20335 20337 20341 20347 20353 20355 20361 20365 20367 20373 20377 20383 20391 203614
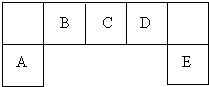 短周期主族元素A、B、C、D、E在元素周期表中的位置如图:请回答下列问题:
短周期主族元素A、B、C、D、E在元素周期表中的位置如图:请回答下列问题: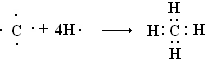
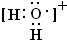
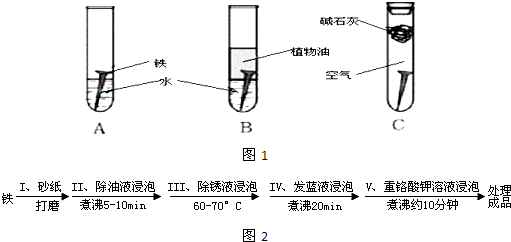
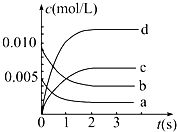 在2L密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如下表所示:
在2L密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如下表所示: