0 20020 20028 20034 20038 20044 20046 20050 20056 20058 20064 20070 20074 20076 20080 20086 20088 20094 20098 20100 20104 20106 20110 20112 20114 20115 20116 20118 20119 20120 20122 20124 20128 20130 20134 20136 20140 20146 20148 20154 20158 20160 20164 20170 20176 20178 20184 20188 20190 20196 20200 20206 20214 203614
 (2012?南京模拟)己二酸是合成尼龙-66的主要原料之一.实验室用高锰酸钾氧化环己醇制己二酸的装置如图所示(加热、搅拌和仪器固定装置均已略去).实验过程如下:
(2012?南京模拟)己二酸是合成尼龙-66的主要原料之一.实验室用高锰酸钾氧化环己醇制己二酸的装置如图所示(加热、搅拌和仪器固定装置均已略去).实验过程如下: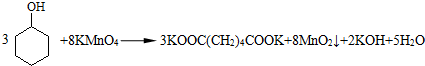
 (2012?南京模拟)三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛应用.它可在铜的催化作用下由F2和过量的NH3反应得到.
(2012?南京模拟)三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛应用.它可在铜的催化作用下由F2和过量的NH3反应得到.