0 19829 19837 19843 19847 19853 19855 19859 19865 19867 19873 19879 19883 19885 19889 19895 19897 19903 19907 19909 19913 19915 19919 19921 19923 19924 19925 19927 19928 19929 19931 19933 19937 19939 19943 19945 19949 19955 19957 19963 19967 19969 19973 19979 19985 19987 19993 19997 19999 20005 20009 20015 20023 203614
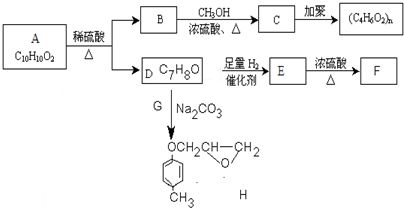


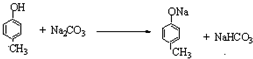
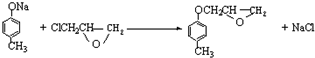
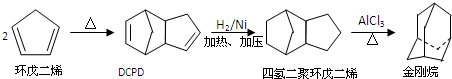
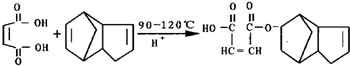
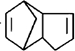
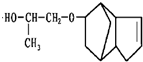
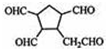
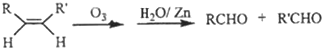 ,请写出下列反应产物的结构简式:
,请写出下列反应产物的结构简式:
 (2012?长宁区二模)三草酸合铁酸钾晶体(K3[Fe(C2O4)3]?xH2O)是一种光敏材料,可用于摄影和蓝色印刷.为测定该晶体中铁的含量和结晶水的含量,某实验小组做了如下实验:
(2012?长宁区二模)三草酸合铁酸钾晶体(K3[Fe(C2O4)3]?xH2O)是一种光敏材料,可用于摄影和蓝色印刷.为测定该晶体中铁的含量和结晶水的含量,某实验小组做了如下实验:

 (2012?长宁区二模)铁是一种重要的金属,它的单质及化合物有着各自的性质.一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g),已知该反应的平衡常数(K)与温度(T)的关系如图所示:
(2012?长宁区二模)铁是一种重要的金属,它的单质及化合物有着各自的性质.一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g),已知该反应的平衡常数(K)与温度(T)的关系如图所示: