0 19480 19488 19494 19498 19504 19506 19510 19516 19518 19524 19530 19534 19536 19540 19546 19548 19554 19558 19560 19564 19566 19570 19572 19574 19575 19576 19578 19579 19580 19582 19584 19588 19590 19594 19596 19600 19606 19608 19614 19618 19620 19624 19630 19636 19638 19644 19648 19650 19656 19660 19666 19674 203614
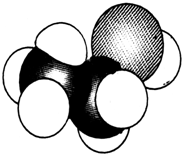 某有机物的分子模型如图所示,则该有机物的名称可能为( )
某有机物的分子模型如图所示,则该有机物的名称可能为( )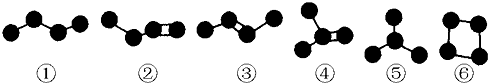
 已知A、B、C、D、E、F为周期表前四周期原子序数依次增大的六种元素.其中A是元素周期表中原子半径最小的元素,B原子最外层电子数是内层电子数的2倍.D、E为同主族元素,且E的原子序数为D的2倍.F元素在地壳中含量位于金属元素的第二位.试回答下列问题:
已知A、B、C、D、E、F为周期表前四周期原子序数依次增大的六种元素.其中A是元素周期表中原子半径最小的元素,B原子最外层电子数是内层电子数的2倍.D、E为同主族元素,且E的原子序数为D的2倍.F元素在地壳中含量位于金属元素的第二位.试回答下列问题:

