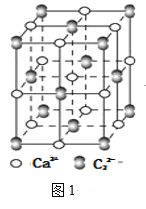
【题目】富硼渣中含有镁硼酸盐(2MgO·B2O3)、镁硅酸盐(2MgO·SiO2)及少量Al2O3、FeO等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸(H3BO3)晶体的一种工艺流程如下:

已知:生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)
Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | |
开始沉淀时 | 1.9 | 3.4 | 7.0 | 9.1 |
完全沉淀时 | 3.2 | 4.7 | 9.0 | 11.1 |
(1)上述流程中能加快反应速率的措施有_____、_____等。
(2)酸浸时发生反应
2MgO·SiO2 +2H2SO4=2MgSO4+SiO2+2H2O,
2MgO·B2O3+2H2SO4+H2O=2H3BO3+2MgSO4。
①上述反应体现出酸性强弱:H2SO4______H3BO3(填“>”或“<”)。
②酸浸时,富硼渣中所含Al2O3和FeO也同时溶解,写出相关反应的离子方程式:___________、____________。
③已知硼酸与过量NaOH溶液发生的中和反应为:H3BO3+OH- =B(OH)4-。下列关于硼酸的说法正确的是_____。
a.硼酸的电离方程式可表示为:H3BO3 + H2O![]() B(OH)4-+H+
B(OH)4-+H+
b.硼酸是一元弱酸
c.向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
(3)检验浸出液中的杂质离子
取少量浸出液,______(填操作和现象),证明溶液中含有Fe2+。
(4)除去浸出液中的杂质离子
用MgO调节溶液的pH至____以上,使杂质离子转化为______(填化学式)沉淀,过滤。
(5)获取晶体
ⅰ.浓缩滤液,使MgSO4和H3BO3接近饱和;
ⅱ.控制温度使两种晶体分别从溶液中结晶。结合下图溶解度曲线,简述ⅱ的方法:将浓缩液加入到高压釜(高压环境可保证在高温条件下水为液态)中,__________(将方法补充完整)。