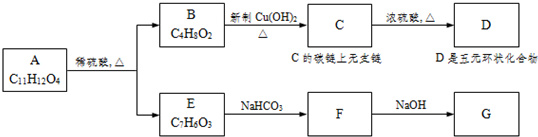
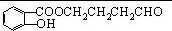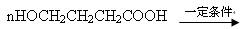0 18962 18970 18976 18980 18986 18988 18992 18998 19000 19006 19012 19016 19018 19022 19028 19030 19036 19040 19042 19046 19048 19052 19054 19056 19057 19058 19060 19061 19062 19064 19066 19070 19072 19076 19078 19082 19088 19090 19096 19100 19102 19106 19112 19118 19120 19126 19130 19132 19138 19142 19148 19156 203614
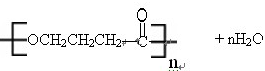
 如图反应是有名的Diels-Alder反应的一个著名化学反应方程式:分析上述有机化学反应,可判断其反应的类型是( )
如图反应是有名的Diels-Alder反应的一个著名化学反应方程式:分析上述有机化学反应,可判断其反应的类型是( )