0 18923 18931 18937 18941 18947 18949 18953 18959 18961 18967 18973 18977 18979 18983 18989 18991 18997 19001 19003 19007 19009 19013 19015 19017 19018 19019 19021 19022 19023 19025 19027 19031 19033 19037 19039 19043 19049 19051 19057 19061 19063 19067 19073 19079 19081 19087 19091 19093 19099 19103 19109 19117 203614
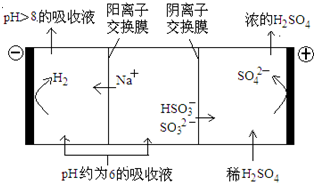 直接排放含SO2的烟气会形成酸雨,危害环境.利用钠碱循环法可脱除烟气中的SO2.
直接排放含SO2的烟气会形成酸雨,危害环境.利用钠碱循环法可脱除烟气中的SO2.