0 18620 18628 18634 18638 18644 18646 18650 18656 18658 18664 18670 18674 18676 18680 18686 18688 18694 18698 18700 18704 18706 18710 18712 18714 18715 18716 18718 18719 18720 18722 18724 18728 18730 18734 18736 18740 18746 18748 18754 18758 18760 18764 18770 18776 18778 18784 18788 18790 18796 18800 18806 18814 203614
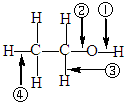 针对如图所示乙醇分子结构,下述关于乙醇在各种化学反应中化学键断裂情况的说法不正确的是( )
针对如图所示乙醇分子结构,下述关于乙醇在各种化学反应中化学键断裂情况的说法不正确的是( )