0 18006 18014 18020 18024 18030 18032 18036 18042 18044 18050 18056 18060 18062 18066 18072 18074 18080 18084 18086 18090 18092 18096 18098 18100 18101 18102 18104 18105 18106 18108 18110 18114 18116 18120 18122 18126 18132 18134 18140 18144 18146 18150 18156 18162 18164 18170 18174 18176 18182 18186 18192 18200 203614
 (2012?闸北区一模)碳酸钠和碳酸氢钠在生产、生活中都有重要的应用.现有3.58g Na2CO3和NaHCO3固体混合物,将其制成溶液后,边搅拌边逐滴滴加80.0mL 1.0mol/L盐酸,反应完全后生成的CO2气体折算成标准状况下的体积为896mL(设气体全部逸出,下同).(1)通过计算可知上述反应中
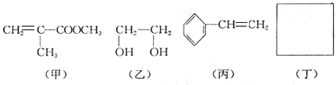
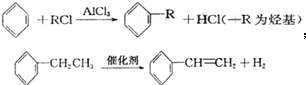
(2012?闸北区一模)碳酸钠和碳酸氢钠在生产、生活中都有重要的应用.现有3.58g Na2CO3和NaHCO3固体混合物,将其制成溶液后,边搅拌边逐滴滴加80.0mL 1.0mol/L盐酸,反应完全后生成的CO2气体折算成标准状况下的体积为896mL(设气体全部逸出,下同).(1)通过计算可知上述反应中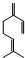 ,一分子该物质与一分子溴发生加成反应的产物(只考虑位置异构)理论上最多有
,一分子该物质与一分子溴发生加成反应的产物(只考虑位置异构)理论上最多有