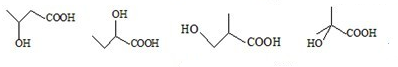
0 17900 17908 17914 17918 17924 17926 17930 17936 17938 17944 17950 17954 17956 17960 17966 17968 17974 17978 17980 17984 17986 17990 17992 17994 17995 17996 17998 17999 18000 18002 18004 18008 18010 18014 18016 18020 18026 18028 18034 18038 18040 18044 18050 18056 18058 18064 18068 18070 18076 18080 18086 18094 203614
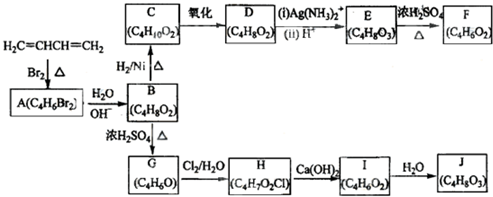
 +H2O
+H2O