能源短缺是人类社会面临的重大问题,利用化学反应可实现多种形式的能量相互转化。请回答以下问题:
(1)由气态基态原子形成1mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是旧键断裂和新键的形成过程。已知反应N2(g)+3H2(g) 2NH3(g) △H=-93 kJ·mol-1。
2NH3(g) △H=-93 kJ·mol-1。
试根据表中所列键能数据,计算a 的数值为 kJ/mol。
化学键 | H-H | N-H | N≡N |
键能/kJ·mol-1 | 436 | a | 945 |
(2)甲醇是一种可再生能源,具有广泛的开发和应用前景。已知在常压下有如下变化:
① 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH =a kJ/mol
② H2O(g)=H2O(l) ΔH =b kJ/mol
写出液态甲醇完全燃烧生成二氧化碳和液态水的热化学方程式: 。
(3)已知:HCN(aq)与NaOH(aq)反应的焓变△H=-12.1kJ·mol-1; HCl(aq)与NaOH(aq)反应的焓变ΔH=-55.6 kJ·mol-1。则HCN在水溶液中电离的焓变ΔH等于 。
(4)已知:H2(g)+1/2O2(g)=H2O(1) △H=-285.83kJ·mol-1
CO(g)+1/2O2(g)=CO2(g) △H=-282.9kJ·mol-1;
若氢气与一氧化碳的混合气体完全燃烧可生成5.4g H2O(l),并放出114.3kJ的热量,则混合气中CO的物质的量为 (计算结果保留以为小数)
在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g) CO(g)+H2O(g),
CO(g)+H2O(g),
其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K = 。
(2)该反应为 反应(选填“吸热”、“放热”)。
(3)能说明该反应达到化学平衡状态的是 。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:3c(CO2)·c(H2)=5c(CO)·c(H2O),试判断此时的温度为 ℃。
(5)830℃时,在1L密闭容器中分别投入lmolH2和1molCO2反应达到化学平街时,CO2的转化率为 保持温度不变.在平衡体系中再充入1molH2和1 molCO2重新达到化学平衡时,CO2 的平衡转化率 (填“增大”“减小”或“不变”)。
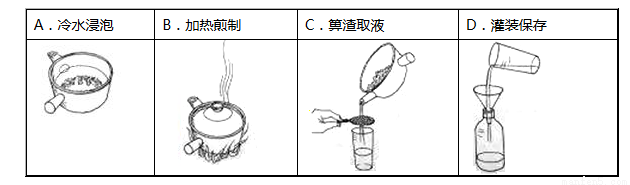
为达到实验目的,下列仪器和药品使用均正确的是 ( )
选项 | 目的 | 仪器 | 药品 |
A | 配制1 mol·L-1NaCl溶液 | 烧杯、玻璃棒、容量瓶、胶头滴管 | 氯化钠、水 |
B | 粗盐提纯 | 烧杯、玻璃棒、长颈漏斗、酒精灯、蒸发皿 | 粗盐、水 |
C | 萃取碘水中的碘 | 烧杯、分液漏斗 | 碘水、乙醇 |
D | 检验集气瓶中的气体是氧气 | 集气瓶(带玻璃片) | 带火星的木条 |
 2c(g)△H<0,下列各图正确的是 ( )
2c(g)△H<0,下列各图正确的是 ( )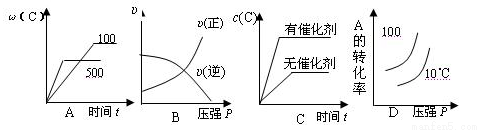
 pC在某温度下达到平衡。
pC在某温度下达到平衡。