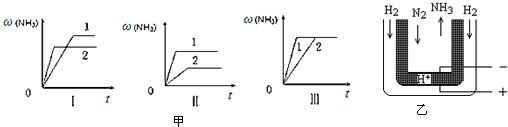
20.现有NH4Cl、K2SO4、(NH4)2SO4 三种化肥,只用下列一种试剂可将它们区别开来的是( )
| A. | CuSO4溶液 | B. | 盐酸 | C. | NaOH溶液 | D. | Ba(OH)2溶液 |
19.开发、使用清洁能源发展“低碳经济”,正成为科学家研究的主要课题.氢气、甲醇是优质的清洁燃料
Ⅰ、已知:①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(g)△H1=-1275.6kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H2=-566.0kJ/mol
③H2O(g)=H2O(1)△H3=-44.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:CH3OH(1)+O2(g)=CO(g)+2H2O(1)△H=-442.8kJ•mol-1.
Ⅱ、工业上采用下列反应合成甲醇:CO(g)+2H2(g)═CH3OH(g)△H=Q kJ/mol
(1)下列一定能说明该可逆反应达到化学平衡状态的是(填字母序号)CD.
A.生成CH3OH的速率与消耗CO的速率相等 B.混合气体的密度不变
C.CH3OH、CO、H2的浓度都不再发生变化 D.混合气体的平均相对分子质量不变
(2)如表所列数据是该可逆反应在不同温度下的化学平衡常数(K).
①由表中数据判断Q<0(填“>”、“<”或“=”).
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应后,达到平衡测得c(CO)=0.2mol/L,此时对应的温度为250℃℃;CO的转化率为80%;
(3)一定温度下,将1mol CO和3molH2分别充入容积均为1L的甲(恒压)、乙(恒容)密闭容器中.若经过60s乙容器中反应达到平衡,则甲容器中达到平衡时所需的时间<60s(填“>”、“<”或“=”).
(4)要提高CO的转化率并且提高反应速率,可采取的措施是D(填字母).
A.升温 B.加入催化剂 C.增加CO的浓度
D.体积不变通入H2 E.体积不变通入惰性气体 F.分离出甲醇.
Ⅰ、已知:①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(g)△H1=-1275.6kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H2=-566.0kJ/mol
③H2O(g)=H2O(1)△H3=-44.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:CH3OH(1)+O2(g)=CO(g)+2H2O(1)△H=-442.8kJ•mol-1.
Ⅱ、工业上采用下列反应合成甲醇:CO(g)+2H2(g)═CH3OH(g)△H=Q kJ/mol
(1)下列一定能说明该可逆反应达到化学平衡状态的是(填字母序号)CD.
A.生成CH3OH的速率与消耗CO的速率相等 B.混合气体的密度不变
C.CH3OH、CO、H2的浓度都不再发生变化 D.混合气体的平均相对分子质量不变
(2)如表所列数据是该可逆反应在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应后,达到平衡测得c(CO)=0.2mol/L,此时对应的温度为250℃℃;CO的转化率为80%;
(3)一定温度下,将1mol CO和3molH2分别充入容积均为1L的甲(恒压)、乙(恒容)密闭容器中.若经过60s乙容器中反应达到平衡,则甲容器中达到平衡时所需的时间<60s(填“>”、“<”或“=”).
(4)要提高CO的转化率并且提高反应速率,可采取的措施是D(填字母).
A.升温 B.加入催化剂 C.增加CO的浓度
D.体积不变通入H2 E.体积不变通入惰性气体 F.分离出甲醇.
18.汽车上的催化转化器可将尾气中的主要污染物转化成无毒物质,反应为:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-aKJ/mol (a>0)在某温度时,用气体传感器测得不同时间的NO和CO浓度如表.经分析,得出结论正确的是( )
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/10-4mol.L-1 | 10.0 | 4.05 | 2.50 | 1.60 | 1.00 | 1.00 |
| c(CO)/10-3mol.L-1 | 3.60 | 3.05 | 2.85 | 2.76 | 2.70 | 2.70 |
| A. | 该反应的平衡常数和转化反应速率在夏季时比冬季时高 | |
| B. | 2~3s间的平均反应速率v(NO)=0.9 moI/(L•s) | |
| C. | 该温度下,此反应的平衡常数K=500 | |
| D. | 若该催化转化器气舱容积为2L,则达到平衡时反应放出热量0.9aJ |
17.一定温度下,在恒容容器中,对于反应2SO2(g)+O2(g)═2SO3(g),SO2和O2起始时分别为20mol和10mol,达到平衡时SO2的转化率为80%.若从SO3开始进行反应,在相同条件下,欲使平衡时各成分的质量分数与前平衡时相同,则起始时SO3的物质的量及SO3的转化率分别为( )
| A. | 10mol和10% | B. | 20mol和40% | C. | 20mol和20% | D. | 30mol和80% |
14.在一定条件下,将3molA和1molB两种其他混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)═xC(g)+2D(s).2min 时该反应达到平衡,生成了0.8molD,并测得C的浓度为0.2mol•L-1.下列判断错误的是( )
0 173806 173814 173820 173824 173830 173832 173836 173842 173844 173850 173856 173860 173862 173866 173872 173874 173880 173884 173886 173890 173892 173896 173898 173900 173901 173902 173904 173905 173906 173908 173910 173914 173916 173920 173922 173926 173932 173934 173940 173944 173946 173950 173956 173962 173964 173970 173974 173976 173982 173986 173992 174000 203614
| A. | x=1 | |
| B. | 充入稀有气体增大体系压强,可提高该反应的反应速率 | |
| C. | 平衡时A与B的转化率相等,均为40% | |
| D. | 平衡时B与C的浓度之比为3:2 |
 Ⅰ.t℃时,将2mol SO2和1mol O2通入体积为2L的恒温恒容密闭容器中,发生如下反应:
Ⅰ.t℃时,将2mol SO2和1mol O2通入体积为2L的恒温恒容密闭容器中,发生如下反应: 工业上以黄铁矿为原料生产硫酸,其中重要的一步是催化氧化(生产中保持恒温恒容条件):2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ•mol-1
工业上以黄铁矿为原料生产硫酸,其中重要的一步是催化氧化(生产中保持恒温恒容条件):2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ•mol-1