8.现有室温下的四种溶液,其pH如表所示,下列有关叙述不正确的是( )
| ① | ② | ③ | ④ | |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | NaOH溶液 | 醋酸 | 盐酸 |
| A. | ③④中分别加入适量醋酸钠晶体,两溶液pH均增大 | |
| B. | ②③两溶液等体积混合,所得溶液中:c(OH-)>c(H+) | |
| C. | 分别加水稀释10倍,溶液的pH:①>②>④>③ | |
| D. | V1L④和V2L①溶液混合后,若pH=7,则V1<V2 |
7.萃取碘水中的碘,可用的萃取剂是①四氯化碳 ②汽油 ③酒精( )
| A. | 只有① | B. | ①和② | C. | ①和③ | D. | ①②③ |
3.下列各组离子一定能大量共存的是( )
| A. | 常温下,pH=12的溶液中:SO32-、Cl-、K+、SiO32- | |
| B. | 在含大量Fe3+的溶液中:NH4+、Na+、Cl-、I- | |
| C. | 在pH=1的溶液中:K+、Fe2+、Cl-、NO3- | |
| D. | 在无色透明溶液中:NH${\;}_{4}^{+}$、Fe3+、SO42-、HCO${\;}_{3}^{-}$ |
2. A、B、C、D是中学化学中常见物质,在一定条件下四者相互转化关系如图所示(部分反应中的水已略去),其中A、B、C均含有同一种元素.下列说法错误的是( )
A、B、C、D是中学化学中常见物质,在一定条件下四者相互转化关系如图所示(部分反应中的水已略去),其中A、B、C均含有同一种元素.下列说法错误的是( )
 A、B、C、D是中学化学中常见物质,在一定条件下四者相互转化关系如图所示(部分反应中的水已略去),其中A、B、C均含有同一种元素.下列说法错误的是( )
A、B、C、D是中学化学中常见物质,在一定条件下四者相互转化关系如图所示(部分反应中的水已略去),其中A、B、C均含有同一种元素.下列说法错误的是( )| A. | 若A为碳单质,则B可以用来灭火 | |
| B. | 若A为AlCl3,D为NaOH,则反应Ⅲ发生的是盐类双水解 | |
| C. | 若A为烧碱,D为CO2,则C的水溶液呈碱性 | |
| D. | 若A为氯水,D为日常生活中用途最广的金属单质,则I、Ⅱ、Ⅲ均是氧化还原反应 |
1.研究氮及其化合物的性质在人类进步过程中具有极为重要的意义.
(1)工业上消除氮的氧化物可采用以下反应:CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)△H
在温度为T1和T2时,分别将0.5mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得NO2的物质的量随时间变化数据如下表:
①温度为T1℃时,0~20min内,v(CH4)=0.0125mol/(L.s).
②T1<T2(填“>”或“<”,下空同);△H<0,判断理由是升高温度,NO2的物质的量增大,平衡逆向移动,正反应为放热反应.
③反应CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)的平衡常数表达式K=$\frac{c({N}_{2})×c(C{O}_{2})×{c}^{2}({H}_{2}O)}{c(C{H}_{4})×{c}^{2}(N{O}_{2})}$,温度为T1℃时,K的值为6.4.
④温度为T2℃时,达平衡后,再向容器中加入0.5mol CH4和1.2mol NO2,达新平衡时CH4的转化率将减小(填“增大”、“减小”或“不变”).
(2)已知反应N2O4(g)?2NO2(g),随温度升高,混合气体的颜色变深.将一定量N2O4气体充入如图绝热容器一段时间后,压缩和拉伸活塞过程中气体的透光率(气体颜色越浅,透光率越大)随时间变化如图所示.

①a点与c点相比,c (NO2)更大的是c,体系温度更低的是a.
②d点,v正(NO2)>v逆(NO2)(填“>”、“<”或“=”).
③下列说法能说明透光率不再发生改变的有ad.
a.气体颜色不再改变 b.△H不再改变
c.v正(N2O4)=2v逆(NO2) d.N2O4的转化率不再改变.
(1)工业上消除氮的氧化物可采用以下反应:CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)△H
在温度为T1和T2时,分别将0.5mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得NO2的物质的量随时间变化数据如下表:
温度/℃ 时间/min | 0 | 10 | 20 | 40 | 50 |
| T1 | 1.2 | 0.9 | 0.7 | 0.4 | 0.4 |
| T2 | 1.2 | 0.8 | 0.56 | … | 0.5 |
②T1<T2(填“>”或“<”,下空同);△H<0,判断理由是升高温度,NO2的物质的量增大,平衡逆向移动,正反应为放热反应.
③反应CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)的平衡常数表达式K=$\frac{c({N}_{2})×c(C{O}_{2})×{c}^{2}({H}_{2}O)}{c(C{H}_{4})×{c}^{2}(N{O}_{2})}$,温度为T1℃时,K的值为6.4.
④温度为T2℃时,达平衡后,再向容器中加入0.5mol CH4和1.2mol NO2,达新平衡时CH4的转化率将减小(填“增大”、“减小”或“不变”).
(2)已知反应N2O4(g)?2NO2(g),随温度升高,混合气体的颜色变深.将一定量N2O4气体充入如图绝热容器一段时间后,压缩和拉伸活塞过程中气体的透光率(气体颜色越浅,透光率越大)随时间变化如图所示.

①a点与c点相比,c (NO2)更大的是c,体系温度更低的是a.
②d点,v正(NO2)>v逆(NO2)(填“>”、“<”或“=”).
③下列说法能说明透光率不再发生改变的有ad.
a.气体颜色不再改变 b.△H不再改变
c.v正(N2O4)=2v逆(NO2) d.N2O4的转化率不再改变.
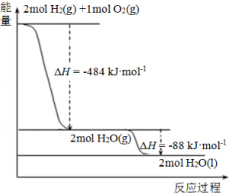
20.已知:H-H、O=O的键能分别是436kJ•mol-1和496kJ•mol-1.依据如图,则H-O的键能是( )
0 173646 173654 173660 173664 173670 173672 173676 173682 173684 173690 173696 173700 173702 173706 173712 173714 173720 173724 173726 173730 173732 173736 173738 173740 173741 173742 173744 173745 173746 173748 173750 173754 173756 173760 173762 173766 173772 173774 173780 173784 173786 173790 173796 173802 173804 173810 173814 173816 173822 173826 173832 173840 203614

| A. | 926 kJ•mol-1 | B. | 485kJ•mol-1 | C. | 463 kJ•mol-1 | D. | 221 kJ•mol-1 |
 电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,除去浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示.
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,除去浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示.