12.已知A(单质)=B(单质),△H>0,则下列判断正确的是( )
| A. | B单质比A单质稳定 | |
| B. | B单质和A单质互为同分异构体 | |
| C. | A单质中化学键的键能比B单质中的大 | |
| D. | 等量的A和B,A单质的内能高 |
11.下列各有机物,在一定条件下自身分子间能发生缩聚反应,而在适宜的条件下分子内又能形成环状结构的是( )
| A. |  | B. | CH3-CH2-CH2-CH2-OH | ||
| C. | CH2=CHCl | D. | 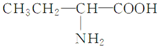 |
10.1932年美国化学家鲍林(L.Pauling)首先提出了电负性的概念.电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值:
请仔细分析,回答下列有关问题:
(1)估计钙元素的电负性的取值范围:0.8<X<1.2.
(2)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中形成的化学键的类型为共价键,其理由是AlCl3中Cl和Al的电负性差值为1.5,而Br的电负性小于Cl,所以AlBr3中两元素的电负性差值小于1.5.
(3)某化合物分子中含有S-N键,你认为该共用电子对偏向于N原子(填元素符号)
| 元素 | H | Li | Be | B | C | N | O | F |
| 电负性 | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
(1)估计钙元素的电负性的取值范围:0.8<X<1.2.
(2)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中形成的化学键的类型为共价键,其理由是AlCl3中Cl和Al的电负性差值为1.5,而Br的电负性小于Cl,所以AlBr3中两元素的电负性差值小于1.5.
(3)某化合物分子中含有S-N键,你认为该共用电子对偏向于N原子(填元素符号)
9. 三氯生是一种抗菌剂,其结构如下图所示,遇含氯自来水能生成有毒的三氯甲烷.下列说法不正确的是( )
三氯生是一种抗菌剂,其结构如下图所示,遇含氯自来水能生成有毒的三氯甲烷.下列说法不正确的是( )
 三氯生是一种抗菌剂,其结构如下图所示,遇含氯自来水能生成有毒的三氯甲烷.下列说法不正确的是( )
三氯生是一种抗菌剂,其结构如下图所示,遇含氯自来水能生成有毒的三氯甲烷.下列说法不正确的是( )| A. | 三氯生的分子式是C12H6Cl3O2 | |
| B. | 三氯甲烷与甲烷均无同分异构体 | |
| C. | 1 mol三氯生最多能与6 mol H2反应 | |
| D. | 三氯生它的相对分子质量为289.5g/mol |
7.下列有关除杂质(括号中为杂质)的操作中,错误的是( )
| A. | 溴苯(液溴):加NaOH溶液,充分振荡,分液,留下层液体 | |
| B. | 乙醇(乙醛):加新制Cu(OH)2溶液,加热至沸腾,过滤取溶液即可 | |
| C. | 乙烷(乙烯):通过盛有足量溴水溶液的洗气瓶洗气 | |
| D. | 乙酸乙酯(乙酸):加饱和碳酸钠溶液,充分振荡,分液,留上层液体 |
6.下列分子式不表示的纯净物的是( )
| A. | C3H8 | B. | C7H8O | C. | CH4O | D. | CH2Cl2 |
5. 某有机物如图所示,该有机物不可能发生的化学反应是( )
某有机物如图所示,该有机物不可能发生的化学反应是( )
①氧化 ②取代 ③加成 ④消去 ⑤还原 ⑥酯化 ⑦水解.
 某有机物如图所示,该有机物不可能发生的化学反应是( )
某有机物如图所示,该有机物不可能发生的化学反应是( )①氧化 ②取代 ③加成 ④消去 ⑤还原 ⑥酯化 ⑦水解.
| A. | ①④ | B. | ⑦ | C. | ②⑤ | D. | ②⑦ |
4.已知次氯酸分子的结构式为H-O-Cl,下列有关说法正确的是( )
0 171722 171730 171736 171740 171746 171748 171752 171758 171760 171766 171772 171776 171778 171782 171788 171790 171796 171800 171802 171806 171808 171812 171814 171816 171817 171818 171820 171821 171822 171824 171826 171830 171832 171836 171838 171842 171848 171850 171856 171860 171862 171866 171872 171878 171880 171886 171890 171892 171898 171902 171908 171916 203614
| A. | 该分子的电子式是H:O:Cl | B. | O原子与H、Cl都形成σ键 | ||
| C. | 该分子为直线型分子 | D. | O原子发生sp杂化 |
 新修改的《机动车驾驶证申领和使用规定》于2010年4月1日起实施,新规规定酒驾一次扣12分,出此拳治理酒驾是因酒后驾车是引发交通事故的重要原因.如图所示为交警在对驾驶员是否饮酒进行检测.其原理是:橙色的酸性K2Cr2O7水溶液遇呼出的乙醇蒸气迅速变蓝,生成蓝绿色的Cr3+.下列对乙醇的描述与此测定原理有关的是( )
新修改的《机动车驾驶证申领和使用规定》于2010年4月1日起实施,新规规定酒驾一次扣12分,出此拳治理酒驾是因酒后驾车是引发交通事故的重要原因.如图所示为交警在对驾驶员是否饮酒进行检测.其原理是:橙色的酸性K2Cr2O7水溶液遇呼出的乙醇蒸气迅速变蓝,生成蓝绿色的Cr3+.下列对乙醇的描述与此测定原理有关的是( )