0 16995 17003 17009 17013 17019 17021 17025 17031 17033 17039 17045 17049 17051 17055 17061 17063 17069 17073 17075 17079 17081 17085 17087 17089 17090 17091 17093 17094 17095 17097 17099 17103 17105 17109 17111 17115 17121 17123 17129 17133 17135 17139 17145 17151 17153 17159 17163 17165 17171 17175 17181 17189 203614



 +NaOH→
+NaOH→ +H2O
+H2O +3Br2→
+3Br2→ ↓+3HB
↓+3HB




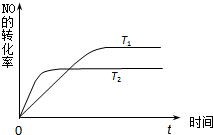 ①由此推知,反应 N2(g)+O2(g)?2NO(g)为(填“吸热”或“放热”)
①由此推知,反应 N2(g)+O2(g)?2NO(g)为(填“吸热”或“放热”)