8.下列叙述正确的是( )
| A. | 蛋白质溶液中加入Na2SO4溶液可使其变性 | |
| B. | 氨基酸具有两性,既能与酸反应又能与碱反应 | |
| C. | 蔗糖既能发生水解反应,又能发生银镜反应 | |
| D. | 纤维素在人体内不能水解生成葡萄糖,因此对人体健康无益 |
7.下列关于油脂的叙述不正确的是( )
| A. | 天然油脂是混和物 | |
| B. | 油脂是天然高分子化合物 | |
| C. | 油脂在碱性溶液中能发生皂化反应 | |
| D. | 人造脂肪是液态的油催化加氢形成的 |
6.某有机物的结构简式如图所示,下列命名正确的是( )


| A. | 2,3,3-三甲基戊烷 | B. | 3,3,4-三甲基己烷 | ||
| C. | 2,3-二甲基-3-乙基丁烷 | D. | 2-乙基-2,3-二甲基丁烷 |
5.下列物质属于同系物的是( )
| A. |  与 与  | B. | CH3CH2Cl与CH2ClCH2CH2Cl | ||
| C. | C2H5OH与CH3OH | D. | CH3CH2CH3与CH2=CHCH3 |
3.两种常见的非金属元素A与B,与常见的三种金属元素C、D、E,A的一种单质是自然界硬度最大的物质,B与C的单质在加热条件下反应生成淡黄色化合物X,D的单质既能与盐酸、也能与NaOH溶液反应生成H2.E的单质与水蒸气反应,生成一种黑色固体Y.请回答下列问题:
(1)X与A的稳定氧化物反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2↑.
(2)将D的单质用砂纸打磨,然后灼烧,液态的D并不滴落的原因Al熔点低,氧化铝熔点高,所以熔化的铝被氧化铝兜着,并不滴落.
(3)ag C的单质投入足量CuSO4溶液中,下列实验现象正确的有BC.
A.钠沉在溶液底部 B.熔化成银色光亮的小球
C.小球四处游动发出”嘶嘶”的声音 D.生成红色固体物质
可能的离子方程式为2Na+Cu2++2H2O=Cu(OH)2↓+2Na++H2↑.将所得沉淀过滤、洗涤、灼烧,可得到$\frac{40a}{23}$g固体.
(4)为探究黑色固体Y的成分,两探究小组分别用黑色固体Y进行以下实验.
①乙组得到的黑色粉末是FeO.
②甲组步骤1中反应的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O.
③乙组步骤4中,溶液变红的原因为Fe2+被氧化为Fe3+,Fe3++遇SCN-显红色;溶液褪色可能的原因是SCN-被过量Cl2氧化;验证方法为向溶液中再加入KSCN溶液,溶液呈红色,则说明之前SCN-被过量Cl2氧化.
(1)X与A的稳定氧化物反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2↑.
(2)将D的单质用砂纸打磨,然后灼烧,液态的D并不滴落的原因Al熔点低,氧化铝熔点高,所以熔化的铝被氧化铝兜着,并不滴落.
(3)ag C的单质投入足量CuSO4溶液中,下列实验现象正确的有BC.
A.钠沉在溶液底部 B.熔化成银色光亮的小球
C.小球四处游动发出”嘶嘶”的声音 D.生成红色固体物质
可能的离子方程式为2Na+Cu2++2H2O=Cu(OH)2↓+2Na++H2↑.将所得沉淀过滤、洗涤、灼烧,可得到$\frac{40a}{23}$g固体.
(4)为探究黑色固体Y的成分,两探究小组分别用黑色固体Y进行以下实验.
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色固体粉末加入稀盐酸 | 溶解,无气泡 | 溶解,无气泡 |
| 2 | 取步骤1中溶液,滴加酸性KMnO4溶液 | 紫色褪去 | 紫色褪去 |
| 3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 |
| 4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变红,后褪色 |
②甲组步骤1中反应的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O.
③乙组步骤4中,溶液变红的原因为Fe2+被氧化为Fe3+,Fe3++遇SCN-显红色;溶液褪色可能的原因是SCN-被过量Cl2氧化;验证方法为向溶液中再加入KSCN溶液,溶液呈红色,则说明之前SCN-被过量Cl2氧化.
1.在给定条件的水溶液中不能大量共存的粒子组是( )
| A. | 通有CO2的溶液:K+、Ca2+、Cl-、NO3- | |
| B. | 既能溶解Al(OH)3又能溶解H2SiO3的溶液中:Na+、CO32-、ClO-、NO3- | |
| C. | 含Fe3+的溶液:Na+、Mg2+、NO3-、I- | |
| D. | CH3COOH溶液:SO42-、Cl-、Cu2+、NH4+ |
20.下列表述正确的是( )
| A. | 体积相等的CO和N2质量一定相等 | |
| B. | 常温常压下,92g的NO2和N2O4混合气体含有的原子数为6 NA | |
| C. | 用过量NaOH溶液吸收 CO2的离子方程式:OH-+CO2=HCO3- | |
| D. | NaHSO4溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀时溶液呈中性 |
19.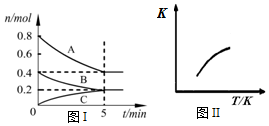 固定容积为2L的密闭容器中发生反应xA(g)+yB(g)?zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系.结合图象判断,下列结论正确的是( )
固定容积为2L的密闭容器中发生反应xA(g)+yB(g)?zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系.结合图象判断,下列结论正确的是( )
0 163491 163499 163505 163509 163515 163517 163521 163527 163529 163535 163541 163545 163547 163551 163557 163559 163565 163569 163571 163575 163577 163581 163583 163585 163586 163587 163589 163590 163591 163593 163595 163599 163601 163605 163607 163611 163617 163619 163625 163629 163631 163635 163641 163647 163649 163655 163659 163661 163667 163671 163677 163685 203614
 固定容积为2L的密闭容器中发生反应xA(g)+yB(g)?zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系.结合图象判断,下列结论正确的是( )
固定容积为2L的密闭容器中发生反应xA(g)+yB(g)?zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系.结合图象判断,下列结论正确的是( )| A. | 200℃时,反应从开始到平衡的平均速率v(A)=0.08 mol•L-1•min-1 | |
| B. | 200℃时,若在第6 min再向体系中充入1 mol He,此时v(正)>v(逆) | |
| C. | 若0~5 min内容器与外界的热交换总量为m kJ,则该反应的热化学方程式可表示为:2A(g)+B(g)?C(g)△H=+5m kJ/mol | |
| D. | 200℃时,平衡后再充入2 mol C,则再次达到平衡时,C的体积分数等于0.25 |
 实验室可用氯酸钾与密度为1.19g•cm-3,溶质质量分数为36.5%的浓盐酸反应制取氯气.
实验室可用氯酸钾与密度为1.19g•cm-3,溶质质量分数为36.5%的浓盐酸反应制取氯气.