17.下列反应的离子方程式正确的是( )
| A. | Mg(HCO3)2溶液与足量的NaOH溶液反应:Mg2++HCO3-+OH-═MgCO3↓+H2O | |
| B. | 向含1 mol KAl(SO4)2的溶液中加入Ba(OH)2溶液至沉淀质量最大时的反应:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O | |
| C. | 向NaHSO4溶液中滴加Ba(OH)2溶液至不再产生沉淀:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| D. | 向Fe(NO3)2和NaBr混合溶液中滴加少量的稀盐酸:6Br-+2NO3-+8H+=3Br2+2NO↑+4H2O |
16.下列实验能达到预期目的是( )
| A. | 用饱和Na2CO3溶液除去SO2气体中含有的少量CO2 | |
| B. | 用加热的方法提取NH4Cl固体中混有的少量单质碘 | |
| C. | 用玻璃棒搅拌漏斗中的液体以加快过滤的速度 | |
| D. | 用醋和KI淀粉溶液检验食用加碘盐中含有的碘元素 |
14.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 0.1mol-NH2中含有的电子数为0.7NA | |
| B. | 标准状况下,2.24L乙醇中含有的C-H数目为0.5NA | |
| C. | 常温常压下,65gZn与足量浓H2SO4充分反应,转移电子数一定为2NA | |
| D. | 2.24LNO与1.12LO2充分反应所得气体中原子数目一定为0.3NA |
13.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 1.0 mol•L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- | |
| B. | 饱和氯水中:NH4+、SO32-、AlO2-、Cl- | |
| C. | 与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- | |
| D. | c(H+)=1.0×10-13mol/L溶液中:K+、Na+、CH3COO-、Br- |
12.下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | 浓硝酸在光照下颜色变黄 | 浓硝酸具有不稳定性 |
| B | 浓硫酸具有酸性和吸水性 | 浓硫酸可使PH试纸先变红后变黑 |
| C | Cl2和SO2均有漂白性 | Cl2和SO2均可使含有酚酞的NaOH溶液褪色 |
| D | C的还原性小于Si | 可用焦炭和石英在高温下反应制取粗硅和CO2 |
| A. | A | B. | B | C. | C | D. | D |
10.下列除杂方案错误的是( )
| 选项 | 被提纯的物质 | 杂质 | 除杂试剂 | 除杂方法 |
| A. | CO(g) | CO2(g) | NaOH 溶液、浓 H2SO4 | 洗气 |
| B. | NH4Cl(aq) | Fe3+(aq) | NaOH溶液 | 过滤 |
| C. | Cl2(g) | HCl(g) | 饱和食盐水、浓H2SO4 | 洗气 |
| D. | Na2CO3(s) | NaHCO3(s) | - | 灼烧 |
| A. | A | B. | B | C. | C | D. | D |
9.下列实验操作能达到实验目的是( )
0 163483 163491 163497 163501 163507 163509 163513 163519 163521 163527 163533 163537 163539 163543 163549 163551 163557 163561 163563 163567 163569 163573 163575 163577 163578 163579 163581 163582 163583 163585 163587 163591 163593 163597 163599 163603 163609 163611 163617 163621 163623 163627 163633 163639 163641 163647 163651 163653 163659 163663 163669 163677 203614
| 选项 | 实验目的 | 实验目的或结论 |
| A | 检验碳与浓硫酸反应后的气体产物 | 将产生的气体依次通过无水CuSO4、澄清石灰水和品红溶液 |
| B | 欲确定磷、砷两元素非金属性的强弱 | 测定同温同浓度的Na3PO4和Na3AsO4水溶液的pH |
| C | 除去Cu粉中混有的CuO | 加入稀硝酸溶液,过滤、洗涤、干燥 |
| D | 制备Fe(OH)3胶体 | 将NaOH浓溶液滴加到饱和FeCl3溶液中 |
| A. | A | B. | B | C. | C | D. | D |
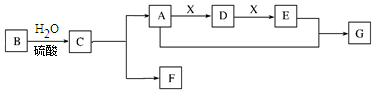

 甲醇是一种优质燃料,在工业上常用
甲醇是一种优质燃料,在工业上常用