9.实验室制备下列气体时,只能用排水法收集的气体是( )
| A. | H2 | B. | NO | C. | NO2 | D. | CO2 |
8.用氨气做喷泉实验,主要利用氨气的性质是( )
| A. | 氧化性 | B. | 还原性 | C. | 极易溶于水 | D. | 溶水成碱性 |
7.某铁红涂料中添加有CuO或FeO中的一种,为探究添加物的成分设计如下实验方案:
(1)请写出实验步骤、预期现象,对应的离子方程式.
(限选试剂:铁粉、3mol/L H2SO4、0.1mol/L酸性KMnO4溶液、10% H2O2、KSCN溶液)
④操作步骤③中反应的离子方程式为5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O.
(2)经分析该铁红涂料中有FeO,为测定铁红中铁的质量分数,兴趣小组的同学称量11.6g该铁红涂料进行了如下实验.
已知:气体由草酸晶体受热分解得到:H2C2O4•2H2O $\frac{\underline{\;\;△\;\;}}{\;}$ CO2↑+CO↑+3H2O.
且除铁红外所用试剂均过量.

①装置A、B中的试剂依次是氢氧化钠溶液、浓硫酸.
②气体通入后,接下来的操作是用点燃的小木条靠近肥皂泡,直到肥皂泡安静燃烧,然后对C装置加热.
③实验前后称得D装置增重8.8g,则此铁红中铁的质最分数是72.41%.
(1)请写出实验步骤、预期现象,对应的离子方程式.
(限选试剂:铁粉、3mol/L H2SO4、0.1mol/L酸性KMnO4溶液、10% H2O2、KSCN溶液)
| 操作步骤 | 预期现象 |
| ①取少量样品于试管中,加入足量的3mol/LH2SO4,充分振荡,将所得澄清的溶液分装在两支试管中. | |
| ②向一支试管中加入足量铁粉,充分振荡;再加入足量3mol/LH2SO4,充分振荡. | 若出现红色固体,则含有CuO. |
| ③向另一支试管中加入0.01mol/L酸性KMnO4溶液. | 若溶液紫红色褪去则含有FeO. |
(2)经分析该铁红涂料中有FeO,为测定铁红中铁的质量分数,兴趣小组的同学称量11.6g该铁红涂料进行了如下实验.
已知:气体由草酸晶体受热分解得到:H2C2O4•2H2O $\frac{\underline{\;\;△\;\;}}{\;}$ CO2↑+CO↑+3H2O.
且除铁红外所用试剂均过量.

①装置A、B中的试剂依次是氢氧化钠溶液、浓硫酸.
②气体通入后,接下来的操作是用点燃的小木条靠近肥皂泡,直到肥皂泡安静燃烧,然后对C装置加热.
③实验前后称得D装置增重8.8g,则此铁红中铁的质最分数是72.41%.
6.设NA代表阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 室温时,1.0L pH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA | |
| B. | 标准状况下,11.2L CH2Cl2中含有的原子数为2.5NA | |
| C. | 1.68g Fe 与足量高温水蒸气反应,转移电子数为0.09NA | |
| D. | 17g H2O2所含非极性键数目为0.5NA |
3.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 在标准状态下,1L庚烷完全燃烧后,所生成的气态产物的分子数为$\frac{7}{22.4}$ NA | |
| B. | 1 mol碳正离子CH5+所含的电子数为10NA | |
| C. | 标准状态下,16 g甲烷完全燃烧所消耗氧气的分子数为NA | |
| D. | 0.5 mol C3H8分子中含C-H共价键2NA |
19.除去下列物质中的杂质(括号内的物质),所使用的试剂和主要操作都正确的是( )
0 163464 163472 163478 163482 163488 163490 163494 163500 163502 163508 163514 163518 163520 163524 163530 163532 163538 163542 163544 163548 163550 163554 163556 163558 163559 163560 163562 163563 163564 163566 163568 163572 163574 163578 163580 163584 163590 163592 163598 163602 163604 163608 163614 163620 163622 163628 163632 163634 163640 163644 163650 163658 203614
| 选项 | 物质 | 使用的试剂 | 主要操作 |
| A | 乙醇(水) | 氧化钙 | 蒸馏 |
| B | 乙酸乙酯(乙酸) | 饱和氢氧化钠溶液 | 分液 |
| C | 苯(苯酚) | 浓溴水 | 过滤 |
| D | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
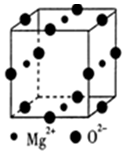 碱土金属指II A族的铍(Be)、镁(Mg)、钙(Ca)、锶(Sr)、钡(Ba)等元素,它们的单质及其化合物有着广泛的用途.
碱土金属指II A族的铍(Be)、镁(Mg)、钙(Ca)、锶(Sr)、钡(Ba)等元素,它们的单质及其化合物有着广泛的用途.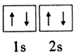 ;镁和铝的笫二电离能:I2(Mg)<I2(Al) (填“>”“<”或“=”).
;镁和铝的笫二电离能:I2(Mg)<I2(Al) (填“>”“<”或“=”).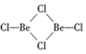 )的形式存在,在1000℃,氯化铍则以BeCl2形式存在.
)的形式存在,在1000℃,氯化铍则以BeCl2形式存在.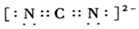 .
. 碳、镁、镍在工业生产和科研领域有广泛用途.请回答下列问题:
碳、镁、镍在工业生产和科研领域有广泛用途.请回答下列问题: )等.
)等. 是常用的分析试剂.其中位于同周期的三种基态原子第一电离能由小到大的顺序为C<O<N(用元素符号表示);这三种元素形成的一种离子与CS2互为等电子体,该离子符号为OCN-.
是常用的分析试剂.其中位于同周期的三种基态原子第一电离能由小到大的顺序为C<O<N(用元素符号表示);这三种元素形成的一种离子与CS2互为等电子体,该离子符号为OCN-.
 短周期元素X、Y的价电子数相同,且原子序数比等于$\frac{1}{2}$;元素Z位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.
短周期元素X、Y的价电子数相同,且原子序数比等于$\frac{1}{2}$;元素Z位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.