15.下列变化不能通过一步反应直接完成的是( )
| A. | Fe→Fe3+ | B. | Fe→Fe3O4 | C. | Al(OH)3→A12O3 | D. | Al→Al(OH)3 |
14.下列各组混合物中,不能用分液漏斗进行分离的是( )
| A. | 水和溴苯 | B. | 乙酸乙酯和饱和碳酸钠溶液 | ||
| C. | 碘和四氯化碳 | D. | 硝基苯和水 |
13.硫一钠原电池具有输出功率较高、循环寿命长等优点.其工作原理可表示为:2Na+xS$?_{充电}^{放电}$Na2Sx.但工作温度过高是这种高性能电池的缺陷.科学家研究发现,采用多硫化合物[如  ]作为电极反应材料,可有效地降低电池的工作温度,且原材料价廉、低毒,具有生物降解性.下列关于此种多硫化合物的叙述正确的是( )
]作为电极反应材料,可有效地降低电池的工作温度,且原材料价廉、低毒,具有生物降解性.下列关于此种多硫化合物的叙述正确的是( )
 ]作为电极反应材料,可有效地降低电池的工作温度,且原材料价廉、低毒,具有生物降解性.下列关于此种多硫化合物的叙述正确的是( )
]作为电极反应材料,可有效地降低电池的工作温度,且原材料价廉、低毒,具有生物降解性.下列关于此种多硫化合物的叙述正确的是( )| A. | 这是一种新型无机非金属材料 | |
| B. | 此化合物可能发生加成反应 | |
| C. | 原电池的负极反应将是单体 转化为 转化为 的过程 的过程 | |
| D. | 当电路中转移0.02mol电子时,将消耗原电池的正极反应材料1.48g |
12.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 2.0 g H218O与D2O的混合物中所含中子数为NA | |
| B. | 足量的铁粉与200 mL 1 mol•L-1的硝酸完全反应,生成H2的分子数为0.1NA | |
| C. | 0.1 mol Cl2通入含0.1 mol FeBr2的溶液中,被氧化的溴离子数为0.2NA | |
| D. | 标准状况下,2.24 L NO和足量O2反应,生成的NO2分子数为0.1NA |
11.X、Y是同主族的非金属元素,如果X原子半径比Y原子半径大,下列说法错误的是( )
| A. | X的非金属性比Y弱 | |
| B. | X的原子序数比Y的大 | |
| C. | X的气态氢化物比Y的气态氢化物稳定 | |
| D. | X的最高价氧化物对应的水化物的酸性比Y的最高价氧化物对应水化物的酸性弱 |
10.下列物质中属于纯净物的是( )
| A. | 天然气 | B. | 铝热剂 | C. | 液态氨 | D. | 氨水 |
9.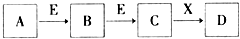 中学常见物质A、B、C、D、E、X,存在下图转化关系(部分生成物和反应条件略去).下列推断不正确的是( )
中学常见物质A、B、C、D、E、X,存在下图转化关系(部分生成物和反应条件略去).下列推断不正确的是( )
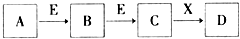 中学常见物质A、B、C、D、E、X,存在下图转化关系(部分生成物和反应条件略去).下列推断不正确的是( )
中学常见物质A、B、C、D、E、X,存在下图转化关系(部分生成物和反应条件略去).下列推断不正确的是( )| A. | 若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁 | |
| B. | 若D为NaOH,则A、B、C均可与X反应生成D | |
| C. | 若D为NaCl,且A可与C反应生成B,则E可能是CO2 | |
| D. | 若D为H2SO4,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C |
8.下列是有关生活中的醋酸,其中主要利用了醋酸酸性的是( )
①醋酸不小心滴到大理石桌面上,桌面失去光泽
②熏醋可一定程度上防止流行性感冒
③醋可以除去水壶上的水垢
④用醋和酒烹饪鱼,除去鱼的腥味.
①醋酸不小心滴到大理石桌面上,桌面失去光泽
②熏醋可一定程度上防止流行性感冒
③醋可以除去水壶上的水垢
④用醋和酒烹饪鱼,除去鱼的腥味.
| A. | ①③④ | B. | ②④ | C. | ①④ | D. | ②③ |
7.设NA为阿伏加德罗常数的值,下列说法正确的是( )
0 163397 163405 163411 163415 163421 163423 163427 163433 163435 163441 163447 163451 163453 163457 163463 163465 163471 163475 163477 163481 163483 163487 163489 163491 163492 163493 163495 163496 163497 163499 163501 163505 163507 163511 163513 163517 163523 163525 163531 163535 163537 163541 163547 163553 163555 163561 163565 163567 163573 163577 163583 163591 203614
| A. | 标准状况下,22.4L苯所含的碳碳双键数为3NA | |
| B. | 常温常压下,28 g乙烯和丙烯(C3H6)的混合气体中所含氢原子数为4NA | |
| C. | 1 mol金属钠在足量乙醇完全反应转移的电子数为2NA | |
| D. | 1 mol•L-1的醋酸溶液中含醋酸分子数为NA |
