3.下列有关说法不正确的是( )
| A. | 氨基酸分子中均含有羧基(-COOH)和氨基(-NH2) | |
| B. | 向鸡蛋白溶液中加入饱和硫酸铵溶液,可观察到蛋白质发生凝聚,再加入蒸馏水,振荡后蛋白质又溶解 | |
| C. | 棉、麻、丝、毛完全燃烧都只生成 CO2 和 H2O | |
| D. | 淀粉在人体内最终水解成葡萄糖 |
2.下列有关减压过滤的说法不正确的是( )
| A. | 减压过滤目的是为了加快过滤速度,得到较干燥的沉淀 | |
| B. | 减压过滤时橡胶插入吸滤瓶内的部分不超过塞子高度的$\frac{2}{3}$ | |
| C. | 减压过滤不宜用于过滤胶状沉淀或颗粒太小的沉淀 | |
| D. | 吸滤完毕后,应先关闭水龙头,再拆下连接抽气泵和吸滤瓶的橡胶管 |
20.在有机合成中,合成高分子的单体或中间体是非常关键的环节.以下是制备甲、乙两种高分子单体原料的合成路线:

已知:
i. $→_{AlCl_{2}}^{RCl}$
$→_{AlCl_{2}}^{RCl}$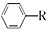
ii. $→_{HCl}^{Fe}$
$→_{HCl}^{Fe}$
iii.R1CH=CHR2$→_{(2)Zn/H_{2}O}^{(1)O_{2}}$R1CHO+R2CHO
iv 1mol B经过上述反应生成2mol C,C不能发生银镜反应.
请回答下列问题:
(1)A的结构简式为 .
.
(2)E→F的反应类型是还原反应.
(3)丙中官能团的名称是羧基、肽键.
(4)下列相关说法中正确的是bc(选填字母序号).
a.B存在顺反异构体
b.甲分子中最多有19个原子共面
c.化合物乙的合成过程中,F→G步骤是为了保护氨基
d.1mol H最多可以和3mol NaOH反应
(5)写出符合下列条件的E的同分异构体的结构简式 .
.
Ⅰ.红外光谱检测表明分子中含有-COOH和-NH2结构;
Ⅱ.1HNMR谱显示分子中含有苯环,且苯环上有两种不同化学环境的氢原子.
(6)写出下列反应的化学方程式:
①A→B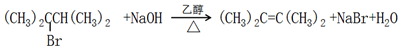 .
.
②由单体乙合成高分子化合物 .
.
(7)大量实验事实表明,当一些基团处于苯环上时,再引入的基团连接位置将受其影响,这种作用称为定位效应.已知一些基团的定位效应如右表.物质丁是乙的一种异构体,其结构差异是苯环上溴原子的位置不同.请以甲苯为起始原料,结合表给信息选用必要的无机试剂合成丁,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).

已知:
i.
 $→_{AlCl_{2}}^{RCl}$
$→_{AlCl_{2}}^{RCl}$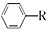
ii.
 $→_{HCl}^{Fe}$
$→_{HCl}^{Fe}$
iii.R1CH=CHR2$→_{(2)Zn/H_{2}O}^{(1)O_{2}}$R1CHO+R2CHO
iv 1mol B经过上述反应生成2mol C,C不能发生银镜反应.
请回答下列问题:
(1)A的结构简式为
 .
.(2)E→F的反应类型是还原反应.
(3)丙中官能团的名称是羧基、肽键.
(4)下列相关说法中正确的是bc(选填字母序号).
a.B存在顺反异构体
b.甲分子中最多有19个原子共面
c.化合物乙的合成过程中,F→G步骤是为了保护氨基
d.1mol H最多可以和3mol NaOH反应
(5)写出符合下列条件的E的同分异构体的结构简式
 .
.Ⅰ.红外光谱检测表明分子中含有-COOH和-NH2结构;
Ⅱ.1HNMR谱显示分子中含有苯环,且苯环上有两种不同化学环境的氢原子.
(6)写出下列反应的化学方程式:
①A→B
 .
.②由单体乙合成高分子化合物
 .
.| 邻对位 定位基 | -CH3、-X、 -NH2、-NHCOR |
| 间位定位基 | -NO2,-COOH |
19.卤素是最活泼的一族非金属,下列关于卤族元素的说法正确的是( )
| A. | 卤素单质的最外层电子数都是7 | |
| B. | 从上到下,卤素原子的电子层数依次增多,半径依次减小 | |
| C. | 从F到I,原子核对最外层电子的吸引能力依次减弱,原子的得电子能力依次减弱 | |
| D. | 卤素单质与H2化合由易到难顺序为F2<Cl2<Br2<I2 |
17.CuCl常用作有机合成催化剂,实验室以初级铜矿粉(主要含Cu2S及少量Fe2O3、FeO等)为原料制备活性CuCl.实验过程如图:
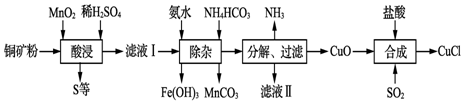
(1)“酸浸”中,加入稀H2SO4不宜过量太多的原因是避免“除杂”步骤消耗更多的氨水和NH4HCO3.
(2)已知:Cu(OH)2可溶于氨水形成深蓝色[Cu(NH3)4]2+溶液.
①“分解”实验条件及现象如表所示.
则“分解”实验条件应选C(填序号).
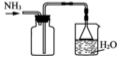
②“分解”生成的NH3可以回收利用.在实验室用图装置来收集NH3,当集气瓶收集满NH3时观察到的现象是漏斗中的液面忽上忽下.
(3)CuCl易氧化,Ksp(CuCl)=1.2×10-6.“合成”中生成CuCl的离子方程式为SO2+2CuO+2Cl-═2CuCl+SO42-;请补充从“合成”所得混合物中得到CuCl的实验操作步骤:过滤、洗涤、真空干燥或隔绝空气干燥
(4)请补充“除杂”步骤中分别回收Fe(OH)3和MnCO3的实验方案:向“滤液Ⅰ”中边搅拌边滴加氨水至溶液pH为[3.2,4.7),将所得沉淀过滤、洗涤、干燥得Fe(OH)3.再向滤液中边搅拌边滴加氨水和碳酸氢铵混合溶液至pH=10,有大量MnCO3沉淀生成,将沉淀过滤、洗涤、干燥得MnCO3.
【已知:pH=3.2时,Fe(OH)3沉淀完全;pH=4.7时,Cu(OH)2开始沉淀;pH=10时,MnCO3沉淀完全】

(1)“酸浸”中,加入稀H2SO4不宜过量太多的原因是避免“除杂”步骤消耗更多的氨水和NH4HCO3.
(2)已知:Cu(OH)2可溶于氨水形成深蓝色[Cu(NH3)4]2+溶液.
①“分解”实验条件及现象如表所示.
| 序号 | 温度/℃ | 压强/kPa | 时间/min | 残液颜色 |
| A | 110 | 101.3 | 60 | 浅蓝色 |
| B | 100 | 74.6 | 40 | 很浅 |
| C | 90 | 60.0 | 30 | 无色透明 |
②“分解”生成的NH3可以回收利用.在实验室用图装置来收集NH3,当集气瓶收集满NH3时观察到的现象是漏斗中的液面忽上忽下.

(3)CuCl易氧化,Ksp(CuCl)=1.2×10-6.“合成”中生成CuCl的离子方程式为SO2+2CuO+2Cl-═2CuCl+SO42-;请补充从“合成”所得混合物中得到CuCl的实验操作步骤:过滤、洗涤、真空干燥或隔绝空气干燥
(4)请补充“除杂”步骤中分别回收Fe(OH)3和MnCO3的实验方案:向“滤液Ⅰ”中边搅拌边滴加氨水至溶液pH为[3.2,4.7),将所得沉淀过滤、洗涤、干燥得Fe(OH)3.再向滤液中边搅拌边滴加氨水和碳酸氢铵混合溶液至pH=10,有大量MnCO3沉淀生成,将沉淀过滤、洗涤、干燥得MnCO3.
【已知:pH=3.2时,Fe(OH)3沉淀完全;pH=4.7时,Cu(OH)2开始沉淀;pH=10时,MnCO3沉淀完全】
14.下列元素的原子半径依次减小的是( )
0 163196 163204 163210 163214 163220 163222 163226 163232 163234 163240 163246 163250 163252 163256 163262 163264 163270 163274 163276 163280 163282 163286 163288 163290 163291 163292 163294 163295 163296 163298 163300 163304 163306 163310 163312 163316 163322 163324 163330 163334 163336 163340 163346 163352 163354 163360 163364 163366 163372 163376 163382 163390 203614
| A. | Na、Mg、Al | B. | N、P、As | C. | P、Si、Al | D. | C、Si、P |
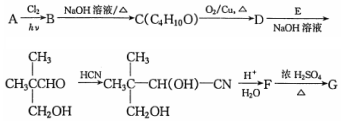
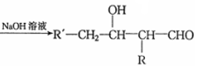
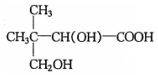 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$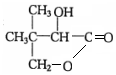 +H2O.F能发生缩聚反应,则生成链节的主链上有四个碳愿子的高分子化合物的结构简式为
+H2O.F能发生缩聚反应,则生成链节的主链上有四个碳愿子的高分子化合物的结构简式为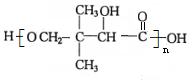 .
.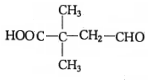 .
.
