17.NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 在1 L 0.2 mol•L-1的Na2CO3溶液中含有CO32-的数目为0.2NA | |
| B. | 0.1 mol Fe参加氧化还原反应,转移的电子数目一定是0.3 NA | |
| C. | 标准状况下22.4 L CH4和C2H4的混合气体所含氢原子数为4NA | |
| D. | 理论上氢氧燃料电池正极消耗11.2 L标准状况下气体时,外线路通过电子数为NA |
16.在下列条件下,两种气体的分子数一定相等的是( )
| A. | 同密度、同压强的 N2 和 C2H4 | B. | 同体积、同密度的C2H4和CO | ||
| C. | 同温度、同体积的 O2和N2 | D. | 同压强、同体积的 O2和 N2 |
15.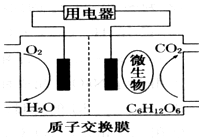 微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示.下列有关微生物电池的说法错误的是( )
微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示.下列有关微生物电池的说法错误的是( )
 微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示.下列有关微生物电池的说法错误的是( )
微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示.下列有关微生物电池的说法错误的是( )| A. | 正极反应中有CO2生成 | |
| B. | O2在正极反应 | |
| C. | H+通过交换膜从负极区移向正极区 | |
| D. | 电池总反应为C6H12O6+6O2═6CO2+6H2O |
14.用NA表示阿伏德罗常数,下列叙述正确的是( )
| A. | 标准状况下,22.4LH2O含有的分子数为 NA | |
| B. | 物质的量浓度为0.5mol•/L的MgCl2溶液中,含有Cl-个数为1 NA | |
| C. | 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA | |
| D. | 通常状况下,NA 个CO2分子占有的体积为22.4L |
13.下列元素的第一电离能最大的是( )
| A. | Be | B. | C | C. | N | D. | O |
12.在水中加入等物质的量的Na+、Ag+、Pb2+和SO42-、Cl-、NO3-,然后放入惰性材料做电极的电解槽中,通电片刻,则氧化产物与还原产物的质量比为 ( )
| A. | 35.5:108 | B. | 16:207 | C. | 8:1 | D. | 108:35.5 |
11.实验室中需要配置2mol/L的NaCl溶液450mL配置时需选用的容量瓶的规格和秤取的NaCl的质量分别是( )
| A. | 450mL 52.65g | B. | 500mL 58.5g | ||
| C. | 500mL 52.65g | D. | 任意规格 58.5g |
10.下列化学用语表达正确的是( )
| A. | 中子数为10的氧原子:${\;}_{10}^{18}$O | B. | 羟基的电子式: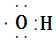 | ||
| C. | Na2S的电子式: | D. | CO2的结构式:O-C-O |
9.下列有关物质的性质和该性质的应用均正确的是( )
| A. | NH3溶于水后显碱性,在FeCl3饱和溶液中通入足量NH3可制取Fe(OH)3胶体 | |
| B. | 碳酸钠溶液显碱性,用热的碳酸钠溶液可去除金属表面的油污 | |
| C. | 氢氟酸具有强酸性,可用于雕刻玻璃 | |
| D. | 铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 |
8.加热N2O5,依次发生分解反应:①N2O5(g)?N2O3(g)+O2(g)、②N2O3(g)?N2O(g)+O2(g).在体积为2L的恒容密闭容器中充入8mol N2O5,加热到T℃时O2和N2O3的物质的量分别为9mol、3.4mol,则T℃时$\frac{c({N}_{2}{O}_{3})•c({O}_{2})}{c({N}_{2}{O}_{5})}$为( )
0 163076 163084 163090 163094 163100 163102 163106 163112 163114 163120 163126 163130 163132 163136 163142 163144 163150 163154 163156 163160 163162 163166 163168 163170 163171 163172 163174 163175 163176 163178 163180 163184 163186 163190 163192 163196 163202 163204 163210 163214 163216 163220 163226 163232 163234 163240 163244 163246 163252 163256 163262 163270 203614
| A. | 10.7 | B. | 8.5 | C. | 9.6 | D. | 10.2 |