4.电解盐酸和氯化铵的混合溶液,发生反应2H++NH4++3Cl-$\frac{\underline{\;电解\;}}{\;}$3H2↑+NCl3,生成VL气体.设NA代表阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 0.1mol•L-1的NH4Cl溶液中含NH4+的数目小于0.01NA | |
| B. | 该反应释放H2的分子数为$\frac{V}{22.4}$NA | |
| C. | 反应中每消耗2molH+转移的电子数为6NA | |
| D. | 120.5gNCl3中所含共价键数为4NA |
3.下列关于乙酸的说法中,错误的是( )
| A. | 乙酸是一种重要的有机酸,常温下是具有刺激性气味的液体 | |
| B. | 乙酸的分子式为C2H4O2,与甲酸(HCOOH)互为同系物 | |
| C. | 乙酸不能被酸性高锰酸钾稀溶液氧化 | |
| D. | 乙酸官能团的结构式为-COOH |
2.纯碱是重要的化工原料,在医药、冶金、化工、食品等领域被广泛使用.
(1)工业生产纯碱的第一步是除去饱和食盐水的中Mg2+、Ca2+离子,从成本角度考虑加入试剂的化学式为Ca(OH)2、Na2CO3.
某实验小组的同学模拟侯德榜制碱法制取纯碱,流程如图1: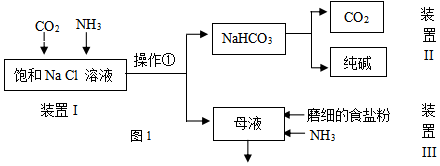
已知:几种盐的溶解度
(2)①写出装置I中反应的化学方程式NaCl+CO2+NH3+H2O=NaHCO3+NH4Cl.
②从平衡移动角度解释该反应发生的原因在溶液中存在下述两种平衡NH3+H2O?NH3•H2O?NH4++OH-,CO2+H2O?H2CO3?H++HCO3-,OH-与H+结合生成水,促进两平衡正向移动,使溶液中的NH4+和HCO3-浓度均增大,由于NaHCO3溶解度小,因此HCO3-与Na+结合生成NaHCO3,固体析出使得反应发生.
③操作①的名称是过滤.
(3)写出装置II中发生反应的化学方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
(4)请结合化学用语说明装置III中加入磨细的食盐粉及NH3的作用.在母液中含有大量的NH4+和Cl-,存在平衡NH4Cl(s)?NH4++Cl-,通入氨气增大NH4+的浓度,加入磨细的食盐粉,增大Cl-的浓度,使上述平衡逆向移动,促使氯化铵结晶析出
(5)该流程中可循环利用的物质是氯化钠和二氧化碳
(6)制出的纯碱中含有杂质NaCl,为测定其纯度,下列方案中不可行的是c.
a.向m克纯碱样品中加入足量CaCl2溶液,测生成CaCO3的质量
b.向m克纯碱样品中加入足量稀H2SO4,干燥后测生成气体的体积
c.向m克纯碱样品中加入足量AgNO3溶液,测生成沉淀的质量.
0 162993 163001 163007 163011 163017 163019 163023 163029 163031 163037 163043 163047 163049 163053 163059 163061 163067 163071 163073 163077 163079 163083 163085 163087 163088 163089 163091 163092 163093 163095 163097 163101 163103 163107 163109 163113 163119 163121 163127 163131 163133 163137 163143 163149 163151 163157 163161 163163 163169 163173 163179 163187 203614
(1)工业生产纯碱的第一步是除去饱和食盐水的中Mg2+、Ca2+离子,从成本角度考虑加入试剂的化学式为Ca(OH)2、Na2CO3.
某实验小组的同学模拟侯德榜制碱法制取纯碱,流程如图1:

已知:几种盐的溶解度
| NaCl | NH4HCO3 | NaHCO3 | NH4Cl | |
| 溶解度(20°C,100gH2O时) | 36.0 | 21.7 | 9.6 | 37.2 |
②从平衡移动角度解释该反应发生的原因在溶液中存在下述两种平衡NH3+H2O?NH3•H2O?NH4++OH-,CO2+H2O?H2CO3?H++HCO3-,OH-与H+结合生成水,促进两平衡正向移动,使溶液中的NH4+和HCO3-浓度均增大,由于NaHCO3溶解度小,因此HCO3-与Na+结合生成NaHCO3,固体析出使得反应发生.
③操作①的名称是过滤.
(3)写出装置II中发生反应的化学方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
(4)请结合化学用语说明装置III中加入磨细的食盐粉及NH3的作用.在母液中含有大量的NH4+和Cl-,存在平衡NH4Cl(s)?NH4++Cl-,通入氨气增大NH4+的浓度,加入磨细的食盐粉,增大Cl-的浓度,使上述平衡逆向移动,促使氯化铵结晶析出
(5)该流程中可循环利用的物质是氯化钠和二氧化碳
(6)制出的纯碱中含有杂质NaCl,为测定其纯度,下列方案中不可行的是c.
a.向m克纯碱样品中加入足量CaCl2溶液,测生成CaCO3的质量
b.向m克纯碱样品中加入足量稀H2SO4,干燥后测生成气体的体积
c.向m克纯碱样品中加入足量AgNO3溶液,测生成沉淀的质量.
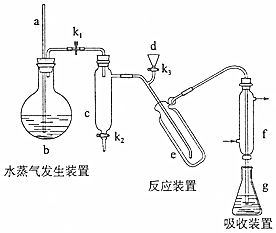
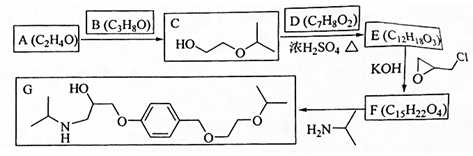
 .
.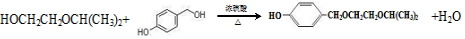 .
.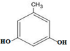 、
、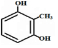 .
. .
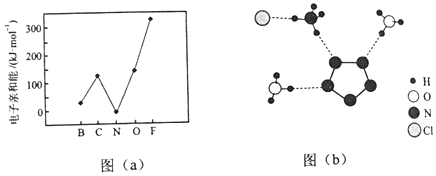
.

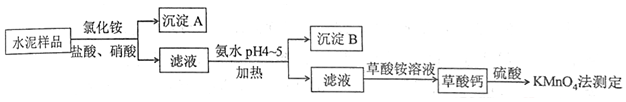
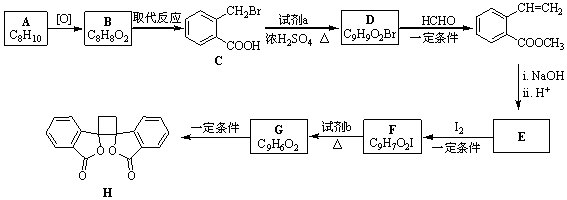
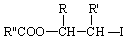
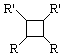
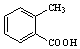 .
.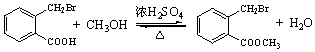 .
. ;此反应同时生成另外一个有机副产物且与F互为同分异构体,此有机副产物的结构简式是
;此反应同时生成另外一个有机副产物且与F互为同分异构体,此有机副产物的结构简式是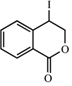 .
.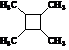 路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).
路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).