16.下列生活用品中主要由合成纤维制造的是( )
| A. | 尼龙绳 | B. | 宣纸 | C. | 羊绒衫 | D. | 棉衬衣 |
15. 改变0.1mol•L-1二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数δ(x)随pH的变化如图所示[已知δ(x)=$\frac{c(X)}{c({H}_{2}A)+c(H{A}^{-})+c({A}^{2-})}$].下列叙述错误的是( )
改变0.1mol•L-1二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数δ(x)随pH的变化如图所示[已知δ(x)=$\frac{c(X)}{c({H}_{2}A)+c(H{A}^{-})+c({A}^{2-})}$].下列叙述错误的是( )
 改变0.1mol•L-1二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数δ(x)随pH的变化如图所示[已知δ(x)=$\frac{c(X)}{c({H}_{2}A)+c(H{A}^{-})+c({A}^{2-})}$].下列叙述错误的是( )
改变0.1mol•L-1二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数δ(x)随pH的变化如图所示[已知δ(x)=$\frac{c(X)}{c({H}_{2}A)+c(H{A}^{-})+c({A}^{2-})}$].下列叙述错误的是( )| A. | pH=1.2时,c(H2A)=c(HA-) | B. | lg[K2(H2A)]=-4.2 | ||
| C. | PH=2.7时,c(HA-)>c(H2A)=c(A2-) | D. | pH=4.2时,c(HA-)=c(A2-)=c(H+) |
14.用电解氧化法可以在铝制品表面形成致密、耐腐蚀的氧化膜,电解质溶液一般为H2SO4-H2C2O4混合溶液.下列叙述错误的是( )
| A. | 待加工铝质工件为阳极 | |
| B. | 可选用不锈钢网作为阴极 | |
| C. | 阴极的电极反应式为:Al3++3e-═Al | |
| D. | 硫酸根离子在电解过程中向阳极移动 |
13.下列说法错误的是( )
| A. | 糖类化合物也可称为碳水化合物 | |
| B. | 维生素D可促进人体对钙的吸收 | |
| C. | 蛋白质是仅由碳、氢、氧元素组成的物质 | |
| D. | 硒是人体必需的微量元素,但不宜摄入过多 |
11.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,足量Fe与22.4 L Cl2反应,转移的电子数为2NA | |
| B. | 0.1molO2完全反应时,转移的电子数一定为 0.4 NA | |
| C. | 用惰性电极电解CuSO4溶液后,如果加入0.1mol Cu(OH)2能使溶液复原,则电路中转移电子的数目为 0.2NA | |
| D. | 常温常压下,100 g 17% H2O2水溶液中含氧原子总数为NA |
10.在一定温度下的恒容密闭容器中,加入等物质的量的A与B物质,A(s)+2B(g)?C(g)+D(g)达到平衡后B的转化率为a,再向容器内加入一定量的B物质达新平衡,下列说法正确的是( )
| A. | 若改为加入A物质可加快反应速率 | |
| B. | 达新平衡后B的转化率减小,A的转化率增大 | |
| C. | 达新平衡后A与B的转化率均增大 | |
| D. | 达新平衡后B的转化率不变,A的转化率增大 |
8.NA代表阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 60g丙醇中含有的共价键的数目为10NA | |
| B. | 在含有1molFeI2 的溶液中,通过足量的氯气,转移的电子数是3NA | |
| C. | 某溶液中Na2CO3和NaHCO3的浓度均为0.1mol/L,Na+离子总数为0.3NA | |
| D. | 50mL 12mol/L 盐酸与足量MnO2共热,转移的电子数为0.3NA |
7.下列说法正确的是( )
0 162989 162997 163003 163007 163013 163015 163019 163025 163027 163033 163039 163043 163045 163049 163055 163057 163063 163067 163069 163073 163075 163079 163081 163083 163084 163085 163087 163088 163089 163091 163093 163097 163099 163103 163105 163109 163115 163117 163123 163127 163129 163133 163139 163145 163147 163153 163157 163159 163165 163169 163175 163183 203614
| A. | 为了防止富脂食品氧化变质,延长食品的保质期,常在包装袋中放入生石灰 | |
| B. | 海水中含有丰富的碘元素,因此碘被称为“海洋元素” | |
| C. | 工业生产玻璃、水泥、漂白粉,均需要用石灰石为原料 | |
| D. | 可以利用氯化铁溶液的酸性清除铜镜表面的铜锈 |
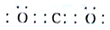 (填电子式)
(填电子式)