3.化学与社会、生产、生活密切相关.下列说法错误的是( )
| A. | 地沟油经过加工处理后,可以用来制肥皂和生物柴油 | |
| B. | PM2.5颗粒(微粒直径约为2.5×10-6m)分散在空气中形成气溶胶 | |
| C. | 采用纳米TiO2光触媒技术,可将装修材料中释放的HCHO转化为无害物质 | |
| D. | 神舟十一号飞船所用太阳能电池板可将光能转换为电能,所用转换材料是硅晶体 |
2.下列有关物质的性质与用途具有对应关系的是( )
| A. | 氮气化学性质通常不活泼,可将炽热的镁粉放在氮气中冷却 | |
| B. | 明矾溶于水能形成胶体,可用于自来水的杀菌消毒 | |
| C. | 常温下铁能被浓硝酸钝化,可用铁质容器贮运浓硝酸 | |
| D. | 金属钠具有强还原性,可用与TiCl4溶液反应制取金属Ti |
1.水是生命之源,下列关于水的说法正确的是( )
| A. | 水是弱电解质 | B. | 可燃冰是可以燃烧的水 | ||
| C. | 氢氧两种元素只能组成水 | D. | 0℃时冰的密度比液态水的密度大 |
20.下列有关化学用语表述正确的是( )
| A. | 1H、2H、3H互为同素异形体 | |
| B. | H2S分子中的化学键为非极性共价键 | |
| C. | S2-的结构示意图: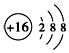 | |
| D. | NH4Cl的电子式: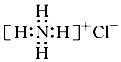 |
19.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1.8 g D2O含有NA个中子 | |
| B. | 标准状况下,22.4 L己烷中共价键数目为19NA | |
| C. | 5.35 g NH4Cl固体中含有N-H键的个数为0.4NA | |
| D. | 常温下将0.1 mol Fe投入足量的浓硝酸中,转移的电子数为0.3NA |
17.有关氢氧燃料电池的电极反应,下列说法正确的是( )
| A. | 电解质为NaCl溶液,正极反应为H2+2e-=2H+ | |
| B. | 电解质为NaOH溶液,正极反应为O2+2e-=2OH- | |
| C. | 电解质为HCl溶液,正极反应为O2+4e-+4H+=2H2O | |
| D. | 电解质为Na2CO3溶液,正极反应为H2+2e-+CO32-=H2O+CO2↑ |
16.ClO2是一种杀菌消毒效率高、二次污染小的水处理剂.实验室中可通过以下反应制得:2KClO3+H2C2O4+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2ClO2↑+K2SO4+2CO2+2H2O↑.下列有关该反应的说法正确的是( )
| A. | H2C2O4是氧化剂 | |
| B. | KClO3是还原剂 | |
| C. | H2C2O4在反应中被氧化 | |
| D. | 1molKClO3参加反应有2mol电子转移 |
15.下列四组能形成原电池且放电后,正极有金属析出的是( )
| A. | Cu、Ag、AgNO3溶液 | B. | Zn、Cu、稀硫酸 | ||
| C. | Fe、Zn、CuSO4溶液 | D. | Fe、C、Fe2(SO4)3溶液 |
14.日常所用干电池其电极分别为碳棒和锌皮,以糊状NH4Cl和ZnCl2作电解质(其中加入MnO2氧化吸收H2),电极反应可简化为:Zn-2e-═Zn2+、2NH4++2e-═2NH3+H2(NH3再用于结合Zn2+)根据上述叙述判断下列说法中正确的是( )
0 162975 162983 162989 162993 162999 163001 163005 163011 163013 163019 163025 163029 163031 163035 163041 163043 163049 163053 163055 163059 163061 163065 163067 163069 163070 163071 163073 163074 163075 163077 163079 163083 163085 163089 163091 163095 163101 163103 163109 163113 163115 163119 163125 163131 163133 163139 163143 163145 163151 163155 163161 163169 203614
| A. | 干电池中Zn为正极,碳为负极 | |
| B. | 干电池可以实现化学能向电能的转化和电能向化学能的转化 | |
| C. | 干电池长时间连续使用时内装糊状物可能流出腐蚀电器 | |
| D. | 干电池工作时,电子由碳极经外电路流向Zn极 |