16.以熔融Na2CO3为电解质,H2和CO混合气为燃料的电池原理如图所示.下列说法正确的是( )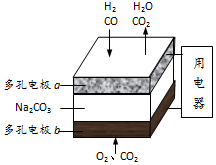

| A. | b是电池的负极 | |
| B. | a电极的反应为:CO+CO32ˉ-2eˉ═2CO2,H2+CO32ˉ-2eˉ═H2O+CO2 | |
| C. | a电极上每消耗22.4L原料气,电池中转移电子数约为2×6.02×1023 | |
| D. | a、b两极消耗的气体的物质的量之比是1:1 |
15.下列有关实验装置(夹持和尾气处理装置已省略)进行的相应实验,不能达到实验目的是( )
| A. | 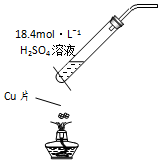 用图装置制取SO2 | |
| B. | 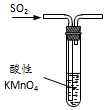 图装置中溶液的颜色变浅,说明SO2具有漂白性 | |
| C. | 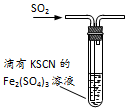 图装置中溶液的颜色变浅,说明SO2具有还原性 | |
| D. |  图装置中产生淡黄色沉淀,说明SO2或H2SO3具有氧化性 |
14.下列指定反应的离子方程式正确的是( )
| A. | 漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- | |
| B. | 银氨溶液中滴加过量的盐酸:Ag(NH3)2++2H+═Ag++2NH4+ | |
| C. | 过量的铁粉与稀硝酸反应:3Fe+2NO3-+8H+═3Fe2++2NO↑+4H2O | |
| D. | 在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3═2FeO42-+3Cl-+H2O+4H+ |
13.物质的性质决定其用途.下列说法正确的是( )
| A. | 二氧化氯具有强氧化性,可用来漂白织物 | |
| B. | 氯化铝是强电解质,可电解其水溶液获得金属铝 | |
| C. | 石英坩埚耐高温,可用来加热熔化烧碱、纯碱等固体 | |
| D. | 铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 |
12.下列有关化学用语表示正确的是( )
| A. | 质量数为35的氯原子:${\;}_{35}^{17}$Cl | |
| B. | NH4Cl的电子式: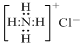 | |
| C. | NaHCO3的水解:HCO3-+H2O?CO32-+H3O+ | |
| D. | 天然橡胶的结构简式: |
10.下列说法正确的是( )
| A. | 铅蓄电池工作时,电解质溶液H2SO4的浓度不变 | |
| B. | 加水稀释0.1 mol•L-1CH3COOH溶液时,CH3COOH的电离程度增大,pH减小 | |
| C. | 在同浓度的盐酸中,ZnS可溶而CuS不溶,说明CuS的溶解度比ZnS的小 | |
| D. | 标准状况下,2.24 LCCl4含有的共价键数为0.4×6.02×1023个 |
9.下列指定反应的离子方程式正确的是( )
| A. | 氯气通入水中:Cl2 +H2O?2H++Cl-+ClO- | |
| B. | 少量的CO2 通入氨水中:CO2+NH3•H2O=NH4++HCO3- | |
| C. | 向NaHSO4溶液中加入过量Ba(OH)2溶液:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| D. | 用稀硝酸除去试管内壁银:3Ag+4H++NO3-═3Ag++NO↑+2H2O |
8.下列关于有机化合物的说法正确的是( )
| A. | 油脂的皂化反应可得到高级脂肪酸与甘油 | |
| B. | 油脂在酸性或碱性条件下均能发生水解反应,且产物相同 | |
| C. | 可以淀粉为原料制取乙酸乙酯 | |
| D. | 油脂的皂化反应属于加成反应 |
7.下表为元素周期表的一部分:
请回答下列问题:
(1)Z元素在周期表中的位置为第三周期ⅦA族.
(2)表中元素原子半径最大的是(写元素符号)Si.
(3)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是ac(填序号).
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1mol硫得电子多
c.Y和硫两元素的简单氢化物受热分解,前者的分解温度高
(4)现有一定量的铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由上表中两种元素组成,气体的相对分子质量都小于50.为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L2.2mol•L-1 NaOH溶液和1molO2,则两种气体的分子式及物质的量分别为NO:0.9mol,NO2:1.3mol,生成硫酸铜物质的量为2mol.
0 162969 162977 162983 162987 162993 162995 162999 163005 163007 163013 163019 163023 163025 163029 163035 163037 163043 163047 163049 163053 163055 163059 163061 163063 163064 163065 163067 163068 163069 163071 163073 163077 163079 163083 163085 163089 163095 163097 163103 163107 163109 163113 163119 163125 163127 163133 163137 163139 163145 163149 163155 163163 203614
| 碳 | 氮 | Y | |
| X | 硫 | Z |
(1)Z元素在周期表中的位置为第三周期ⅦA族.
(2)表中元素原子半径最大的是(写元素符号)Si.
(3)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是ac(填序号).
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1mol硫得电子多
c.Y和硫两元素的简单氢化物受热分解,前者的分解温度高
(4)现有一定量的铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由上表中两种元素组成,气体的相对分子质量都小于50.为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L2.2mol•L-1 NaOH溶液和1molO2,则两种气体的分子式及物质的量分别为NO:0.9mol,NO2:1.3mol,生成硫酸铜物质的量为2mol.