4.下列各组原子中,彼此化学性质一定相似的是( )
| A. | 原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子 | |
| B. | 原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子 | |
| C. | 2p轨道上有一个空轨道的X原子与3p轨道上有一个空轨道的Y原子 | |
| D. | 最外层都只有一个电子的X、Y原子 |
3.某物质中可能有甲酸、乙酸、甲醇和甲酸乙酯1种物质中1种或几种,在鉴别时有下列现象:(1)有银镜反应;(2)加入新制Cu(OH)2悬浊液沉淀不溶解;(3)与含酚酞的NaOH溶液共热发现溶液中红色逐渐消失以至无色,下列叙述正确的有( )
| A. | 几种物质都有 | B. | 有甲酸乙酯,可能有甲酸 | ||
| C. | 有甲酸乙酯和甲醇 | D. | 有甲酸乙酯,可能有甲醇 |
2.氢、氧两种元素组成的常见物质有H2O和H2O2,二者在一定条件下均可分解.
(1)已知:
①H2O的电子式是 .
.
②H2O(g)分解的热化学方程式是2H2O(g)=2H2(g)+O2(g)△H=+482KJ/mol.
③11.2L(标准状况)的H2完全燃烧,生成气态水,放出120.5kJ的热量.
(2)某同学以H2O2分解为例,探究浓度与溶液酸碱性对反应速率的影响.常温下,按照如表所示的方案完成实验.
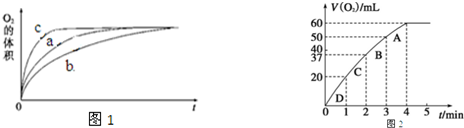
①测得实验a、b、c中生成氧气的体积随时间变化的关系如图1所示.由该图能够得出的实验结论是
其他条件不变时,在碱性环境下加快H2O2的分解速率,酸性环境下减缓H2O2的分解速率.
②测得实验d在标准状况下放出氧气的体积随时间变化的关系如图2所示.解释反应速率变化的原因
随着反应的进行,H2O2的浓度逐渐减小,H2O2的分解速率逐渐减慢;计算H2O2的初始物质的量浓度为0.11 mol•L-1 (保留两位有效数字).
(1)已知:
| 化学键 | 断开1mol化学键所需的能量(kJ) |
| H-H | 436 |
| O-H | 463 |
| O=O | 498 |
 .
.②H2O(g)分解的热化学方程式是2H2O(g)=2H2(g)+O2(g)△H=+482KJ/mol.
③11.2L(标准状况)的H2完全燃烧,生成气态水,放出120.5kJ的热量.
(2)某同学以H2O2分解为例,探究浓度与溶液酸碱性对反应速率的影响.常温下,按照如表所示的方案完成实验.
| 实验编号 | 反应物 | 催化剂 | |
| a | 50mL 5% H2O2溶液 | 1mL 0.1mol•L-1 FeCl3溶液 | |
| b | 50mL 5% H2O2溶液 | 少量浓盐酸 | 1mL 0.1mol•L-1 FeCl3溶液 |
| c | 50mL 5% H2O2溶液 | 少量浓NaOH溶液 | 1mL 0.1mol•L-1 FeCl3溶液 |
| d | 50mL 5% H2O2溶液 | MnO2 | |
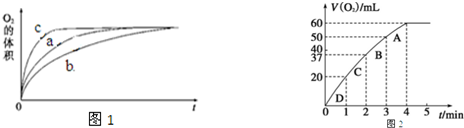
①测得实验a、b、c中生成氧气的体积随时间变化的关系如图1所示.由该图能够得出的实验结论是
其他条件不变时,在碱性环境下加快H2O2的分解速率,酸性环境下减缓H2O2的分解速率.
②测得实验d在标准状况下放出氧气的体积随时间变化的关系如图2所示.解释反应速率变化的原因
随着反应的进行,H2O2的浓度逐渐减小,H2O2的分解速率逐渐减慢;计算H2O2的初始物质的量浓度为0.11 mol•L-1 (保留两位有效数字).
1.部分有机物分子会产生互变异构,如苯与棱晶烷、降冰片二烯与四环烷均能发生互变异构体:

棱晶烷和四环烷的二氯代物的同分异构体数目分别为( )
0 162876 162884 162890 162894 162900 162902 162906 162912 162914 162920 162926 162930 162932 162936 162942 162944 162950 162954 162956 162960 162962 162966 162968 162970 162971 162972 162974 162975 162976 162978 162980 162984 162986 162990 162992 162996 163002 163004 163010 163014 163016 163020 163026 163032 163034 163040 163044 163046 163052 163056 163062 163070 203614

棱晶烷和四环烷的二氯代物的同分异构体数目分别为( )
| A. | 2,7 | B. | 2,8 | C. | 3,7 | D. | 3,8 |