3.某有机物的结构简式为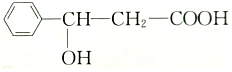 ,对该有机物的下列说法中正确的是( )
,对该有机物的下列说法中正确的是( )
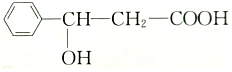 ,对该有机物的下列说法中正确的是( )
,对该有机物的下列说法中正确的是( )| A. | 含有羟基、苯基、羧基三种官能团 | B. | 属于芳香烃 | ||
| C. | 在一定条件下,能发生酯化反应 | D. | 属于羧基,也属于酚类 |
2.已知X、Y、Z都是短周期元素,它们的原子序数依次递增,X原子的电子层数与它的核外电子总数相等,而Z原子的最外层电子数是次外层的3倍,Y和Z可以形成两种以上气态化合物,则下列说法错误的是( )
| A. | Y和Z可以组成元素质量比为7:16的化合物 | |
| B. | X和Y可以组成原子个数比分别为3:l和2:l的两种化合物 | |
| C. | 由X、Y、Z三种元素中任意两种组成的具有10电子的微粒多于2种 | |
| D. | X、Y、Z只能组成一种盐,其中X、Y、Z原子个数比为4:2:3 |
1.短周期元素X、Y、Z、M的原子序数依次增大,原子X的L层电子数是K层的2倍,Y2+电子层结构与氖相同,Z原子的质子数为偶数,室温下M单质为淡黄色固体,下列有关说法正确的是( )
| A. | X、Y、Z、M的原子半径依次减小 | |
| B. | Y与M组成化合物的熔点高于X与M组成的化合物 | |
| C. | X、Z、M的最低价气态氢化物的热稳定性依次增强 | |
| D. | X的单质与Y、Z的最高价氧化物均能发生置换反应 |
20. 汽车尾气是导致雾霾天气的重要源头之一,其含有的NO(g)和CO(g)在一定温度和催化剂条件下可发生反应.
汽车尾气是导致雾霾天气的重要源头之一,其含有的NO(g)和CO(g)在一定温度和催化剂条件下可发生反应.
(一)已知:反应l:N2(g)+O2(g)═2NO(g)△H1 K1
反应2:CO(g)+$\frac{1}{2}$O2(g)═CO2 (g)△H2 K2
反应3:2NO(g)+2CO(g)═N2(g)+CO2(g)△H3 K3
则反应3的焓变△H3=2△H2-△H1(用△H1和△H2表示) 平衡常数K3=$\frac{{{K}_{2}}^{2}}{{K}_{1}}$(用K1和K2表示).
(二)向1.0L恒容密闭容器中,充入N2O(g)和CO(g),可发生如下反应:N2O(g)+CO(g)?N2(g)+CO2(g),所得实验数据如表:
上述实验编号①中,若10min时测得n(N2)=0.12mol,则0至10min内,用CO2表示的平均反应速率以v(CO2)=0.012mol•(L•min)-1;
(2)500℃时,欲使N2O的平衡转化率a(N2O)≥80%,则起始时n(N2O):n(CO)≤1:4.
(3)上述实验编号④达平衡时,b<0.24(填“>”、“<”或“=”),原因是该反应△H<0,升高温度,平衡向逆反应方向移动,故b<0.24mol.
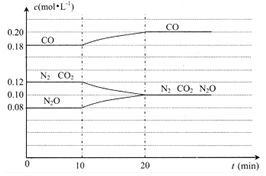
(4)N2O(g)+CO(g)?N2(g)+CO2(g)的反应体系达到平衡后,各物质的浓度在不同条件下的变化情况如如图所示:
①若在第10min仅改变了一个条件,第20min时是在新条件下达到新的平衡状态,则第10min 时改变的条件可能是升温;
②比较CO在第5min和第25min时速率的大小v(5)<v(25)(填”>”、“<”或“=”),你判断的理由是相对于第5min而言,在第10min时升高了温度,且浓度增加了,在其它条件不变时,速率会变快.
 汽车尾气是导致雾霾天气的重要源头之一,其含有的NO(g)和CO(g)在一定温度和催化剂条件下可发生反应.
汽车尾气是导致雾霾天气的重要源头之一,其含有的NO(g)和CO(g)在一定温度和催化剂条件下可发生反应.(一)已知:反应l:N2(g)+O2(g)═2NO(g)△H1 K1
反应2:CO(g)+$\frac{1}{2}$O2(g)═CO2 (g)△H2 K2
反应3:2NO(g)+2CO(g)═N2(g)+CO2(g)△H3 K3
则反应3的焓变△H3=2△H2-△H1(用△H1和△H2表示) 平衡常数K3=$\frac{{{K}_{2}}^{2}}{{K}_{1}}$(用K1和K2表示).
(二)向1.0L恒容密闭容器中,充入N2O(g)和CO(g),可发生如下反应:N2O(g)+CO(g)?N2(g)+CO2(g),所得实验数据如表:
| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(N2O) | n(CO) | n(CO2) | ||
| ① | 400 | 0.20 | 0.30 | 0.14 |
| ② | 500 | 0.10 | 0.40 | 0.080 |
| ③ | 500 | 0.30 | 0.20 | A |
| ④ | 600 | 0.60 | 0.40 | B |
(2)500℃时,欲使N2O的平衡转化率a(N2O)≥80%,则起始时n(N2O):n(CO)≤1:4.
(3)上述实验编号④达平衡时,b<0.24(填“>”、“<”或“=”),原因是该反应△H<0,升高温度,平衡向逆反应方向移动,故b<0.24mol.
(4)N2O(g)+CO(g)?N2(g)+CO2(g)的反应体系达到平衡后,各物质的浓度在不同条件下的变化情况如如图所示:
①若在第10min仅改变了一个条件,第20min时是在新条件下达到新的平衡状态,则第10min 时改变的条件可能是升温;
②比较CO在第5min和第25min时速率的大小v(5)<v(25)(填”>”、“<”或“=”),你判断的理由是相对于第5min而言,在第10min时升高了温度,且浓度增加了,在其它条件不变时,速率会变快.
19.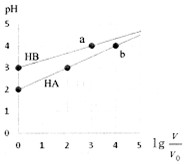 室温下,浓度均为0.1mol•L-1、体积均为V0HA、HB溶液,分别加水稀释至V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列说法正确的是( )
室温下,浓度均为0.1mol•L-1、体积均为V0HA、HB溶液,分别加水稀释至V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列说法正确的是( )
 室温下,浓度均为0.1mol•L-1、体积均为V0HA、HB溶液,分别加水稀释至V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列说法正确的是( )
室温下,浓度均为0.1mol•L-1、体积均为V0HA、HB溶液,分别加水稀释至V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列说法正确的是( )| A. | HA为强酸,HB为弱酸 | |
| B. | 水的电离程度a点大于b点 | |
| C. | 当pH=2时,HA溶液中$\frac{c(HA)}{c({A}^{-})}$=9 | |
| D. | 等浓度等体积的HB与Na0H溶液充分反应后,离子浓度关系大小为:c(B-)>c(Na+)>c(H+)>c(OH-) |
18.直接电解吸收是烟气脱硝的一种有效方法,用6%的稀硝酸吸收NOx会生成亚硝酸,再将吸收液导入电解槽使之转化为硝酸.电解装置如下:下列说法不正确的是( )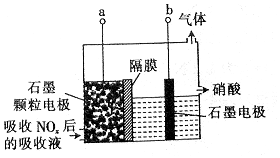

| A. | 吸收NOx的过程涉及氧化还原反应 | |
| B. | 石墨电极为颗粒状,可增大接触面积,提高电解效率 | |
| C. | 当b极上产生2.8 L(标准状况)H2时,转移的电子数为0.5NA(设NA为阿伏加德罗常数的数值) | |
| D. | a极的电极反应式为HNO2-2e-+H2O═3H++NO3- |
17.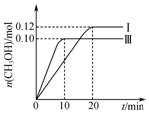 一定温度下,在三个容积均为2.0L的恒容密闭容器中发生反应:CO(g)+2H2(g)?CH3OH(g),各容器中起始物质的物质的量与反应温度见表,反应过程中容器Ⅰ、Ⅲ中CH3OH的物质的量随时间变化关系如图所示:下列说法正确的是( )
一定温度下,在三个容积均为2.0L的恒容密闭容器中发生反应:CO(g)+2H2(g)?CH3OH(g),各容器中起始物质的物质的量与反应温度见表,反应过程中容器Ⅰ、Ⅲ中CH3OH的物质的量随时间变化关系如图所示:下列说法正确的是( )
 一定温度下,在三个容积均为2.0L的恒容密闭容器中发生反应:CO(g)+2H2(g)?CH3OH(g),各容器中起始物质的物质的量与反应温度见表,反应过程中容器Ⅰ、Ⅲ中CH3OH的物质的量随时间变化关系如图所示:下列说法正确的是( )
一定温度下,在三个容积均为2.0L的恒容密闭容器中发生反应:CO(g)+2H2(g)?CH3OH(g),各容器中起始物质的物质的量与反应温度见表,反应过程中容器Ⅰ、Ⅲ中CH3OH的物质的量随时间变化关系如图所示:下列说法正确的是( )| 容器 | 温度/℃ | 起始物质的量/mol | ||
| CO(g) | H2(g) | CH3OH(g) | ||
| Ⅰ | T1 | 0.2 | 0.4 | 0 |
| Ⅱ | T1 | 0 | 0 | 0.4 |
| Ⅲ | T2 | 0.2 | 0.4 | 0 |
| A. | 在前20 min内,容器Ⅰ中反应的平均速率为v(H2)=0.012 mol•L-1•min-1 | |
| B. | 达到平衡后,容器Ⅰ中再充入0.20 mol CO和0.20 mol CH3OH,此时v(正)>v(逆) | |
| C. | 达到平衡时,容器Ⅱ中的压强一定大于容器Ⅰ中的压强的两倍 | |
| D. | 将容器Ⅲ改为绝热容器,实验起始温度为T2,达到平衡时,CO的转化率小于50% |
16.不考虑羟基与氯原子在同一个碳原子上时,有机物C4H9C1O的同分异构体中能与Na反应放出氢气的共有(不含立体异构)( )
| A. | 9 种 | B. | 10种 | C. | 11 种 | D. | 12 种 |
15.X、Y、Z、R是短周期主族元素,X元素是形成有机化合物的必需元素,Y元素的原子最外层电子数是次外层的三倍,Z元素的原子半径是短周期元素中最大的,R原子的核外电子数是X原子核Z原子的核外电子数之和.下列叙述不正确的是( )
0 162862 162870 162876 162880 162886 162888 162892 162898 162900 162906 162912 162916 162918 162922 162928 162930 162936 162940 162942 162946 162948 162952 162954 162956 162957 162958 162960 162961 162962 162964 162966 162970 162972 162976 162978 162982 162988 162990 162996 163000 163002 163006 163012 163018 163020 163026 163030 163032 163038 163042 163048 163056 203614
| A. | XY2是形成酸雨的主要污染物 | |
| B. | X、Y、R三种元素的非金属性Y>R>X | |
| C. | X、Z分别与R形成的化合物中化学键类型不同 | |
| D. | 含有Y、Z、R三种元素的化合物溶液可能显碱性 |