5.室温时,pH=13的强碱溶液和pH=2的强酸溶液混合后,得到混合溶液的pH=12,则强碱与强酸的体积比为( )
| A. | 10:1 | B. | 1:10 | C. | 9:2 | D. | 2:9 |
4.为了达到如表所列的一些有关家庭常用物质的实验要求,请选择合适的化学试剂,将其序号填入对应的表格中对应位置.(供选择的化学试剂如下)
①硝酸银溶液和稀硝酸 ②浓硫酸 ③苯 ④无水硫酸铜粉末
①硝酸银溶液和稀硝酸 ②浓硫酸 ③苯 ④无水硫酸铜粉末
| 实验要求 | 化学试剂 |
| (1)检验酒精中是否有水 | ④ |
| (2)吸收CO中的H2O | ② |
| (3)验证味精中是否有食盐 | ① |
| (4)分离碘水中的碘 | ③ |
1.不同元素的原子在分子内吸引电子的能力大小可用一数值X来表示,若X越大,则原子吸引电子的能力越强,在所形成的分子中成为负电荷一方.下面是某些短周期元素的X值.
(1)通过分析X值的变化规律,确定N、Mg的X值范围:0.93<X(Mg)<1.57;2.55<X(N)<3.44.
(2)推测X值与原子半径的关系是同周期(或同主族)元素,x值越大,原子半径越小.
(3)某有机物结构简式为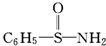 ,在S~N中,你认为共用电子对偏向谁?氮(写原子名称).
,在S~N中,你认为共用电子对偏向谁?氮(写原子名称).
(4)经验规律告诉我们当成键的两原子相应元素电负性的差值△X>1.7时,一般为离子键,当△X<1.7时,一般为共价键,试推断AlBr3中化学键的类型是共价键
(5)预测元素周期表中,X值最小的元素位置第六周期第ⅠA族(放射性元素除外).
| 元素 | Li | Be | B | C | O | F |
| X值 | 0.98 | 1.57 | 2.04 | 2.53 | 3.44 | 3.98 |
| 元素 | Na | Al | Si | P | S | Cl |
| X值 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(2)推测X值与原子半径的关系是同周期(或同主族)元素,x值越大,原子半径越小.
(3)某有机物结构简式为
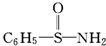 ,在S~N中,你认为共用电子对偏向谁?氮(写原子名称).
,在S~N中,你认为共用电子对偏向谁?氮(写原子名称).(4)经验规律告诉我们当成键的两原子相应元素电负性的差值△X>1.7时,一般为离子键,当△X<1.7时,一般为共价键,试推断AlBr3中化学键的类型是共价键
(5)预测元素周期表中,X值最小的元素位置第六周期第ⅠA族(放射性元素除外).
8.化学已渗透到人类生活的各个方面,下列说法正确的是( )
| A. | 在日常生活中,化学腐蚀是造成钢铁腐蚀的主要原因 | |
| B. | 人造纤维、合成纤维和光导纤维都是有机离分子化合物 | |
| C. | 纤维素在人体内可水解为葡萄糖,故可作人类的营养物质 | |
| D. | 可用Si2N4、Al2O3制作高温结构陶瓷制品 |
6.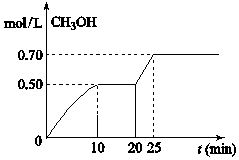 在容积固定为2L的密闭容器中,充入2molCO2和6molH2,在温度500℃时发生反应,CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H<0,CH3OH的浓度随时间变化如右图,下列说法正确的是( )
在容积固定为2L的密闭容器中,充入2molCO2和6molH2,在温度500℃时发生反应,CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H<0,CH3OH的浓度随时间变化如右图,下列说法正确的是( )
 在容积固定为2L的密闭容器中,充入2molCO2和6molH2,在温度500℃时发生反应,CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H<0,CH3OH的浓度随时间变化如右图,下列说法正确的是( )
在容积固定为2L的密闭容器中,充入2molCO2和6molH2,在温度500℃时发生反应,CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H<0,CH3OH的浓度随时间变化如右图,下列说法正确的是( )| A. | 从开始到25分钟,CO2的转化率是35% | |
| B. | 从20分钟到25分钟,可能是缩小容器体积 | |
| C. | 其它条件不变,将温度升到800℃,平衡常数增大 | |
| D. | 从反应开始到10分钟,H2的平均反应速率v(H2)=0.15mol(L•min) |
5.X、Y、Z、W为原子序数依次增大的四种第三周期元素,其单质及其化合物的性质或结构信息如表所示,用化学用语回答下列问题.
请按要求回答下列问题:
(1)工业上制取X的单质的化学方程式:MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑.
(2)X、Y、W三种元素对应的离子半径由大到小的顺序为:Cl->Mg2+>Al3+.
(3)在25℃、101kPa下,已知13.5g的Y的固体单质在W的气体单质中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式是2Al(s)+3Cl2(g)=2AlCl3(s)△H=-1676kJ/mol.
(4)甲中各原子都满足8电子稳定结构,其电子式为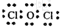 ;
;
(5)Sn与元素Z同主族,周期数比元素Z的大2.则Sn的原子序数为50;已知锡在水溶液中有Sn2+、Sn4+两种存在形式,且硫酸盐均可溶.酸性条件下,SnSO4可用作双氧水的去除剂,试写出所发生反应的离子方程式:Sn2++H2O2+2H+═Sn4++2H2O.潮湿环境中,镀锡铜如果锡层破损不能(填“能”或“不能”)形成铜绿.
| 元素 | X | Y | Z | W |
| 性质 结构 信息 | 工业上常用电解熔融XW2制取X的单质. | Y的最外层电子数比最内层电子数多1. | Z的最高价氧化物的水化物经聚合、脱水,可作袋装食品干燥剂. | W的一种气态氧化物甲对空气的相对密度为3,它溶于水得到单一溶质的弱酸性溶液(有漂白性),该溶液光照后酸性增强. |
(1)工业上制取X的单质的化学方程式:MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑.
(2)X、Y、W三种元素对应的离子半径由大到小的顺序为:Cl->Mg2+>Al3+.
(3)在25℃、101kPa下,已知13.5g的Y的固体单质在W的气体单质中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式是2Al(s)+3Cl2(g)=2AlCl3(s)△H=-1676kJ/mol.
(4)甲中各原子都满足8电子稳定结构,其电子式为
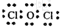 ;
;(5)Sn与元素Z同主族,周期数比元素Z的大2.则Sn的原子序数为50;已知锡在水溶液中有Sn2+、Sn4+两种存在形式,且硫酸盐均可溶.酸性条件下,SnSO4可用作双氧水的去除剂,试写出所发生反应的离子方程式:Sn2++H2O2+2H+═Sn4++2H2O.潮湿环境中,镀锡铜如果锡层破损不能(填“能”或“不能”)形成铜绿.
4.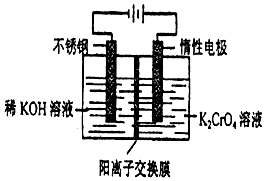 以10L 0.1mol/L铬酸钾(K2CrO4)溶液为原料,电化学法制备重铬酸钾(K2Cr2O7)的实验装置示意图如下,下列说法不正确的是( )
以10L 0.1mol/L铬酸钾(K2CrO4)溶液为原料,电化学法制备重铬酸钾(K2Cr2O7)的实验装置示意图如下,下列说法不正确的是( )
0 162844 162852 162858 162862 162868 162870 162874 162880 162882 162888 162894 162898 162900 162904 162910 162912 162918 162922 162924 162928 162930 162934 162936 162938 162939 162940 162942 162943 162944 162946 162948 162952 162954 162958 162960 162964 162970 162972 162978 162982 162984 162988 162994 163000 163002 163008 163012 163014 163020 163024 163030 163038 203614
 以10L 0.1mol/L铬酸钾(K2CrO4)溶液为原料,电化学法制备重铬酸钾(K2Cr2O7)的实验装置示意图如下,下列说法不正确的是( )
以10L 0.1mol/L铬酸钾(K2CrO4)溶液为原料,电化学法制备重铬酸钾(K2Cr2O7)的实验装置示意图如下,下列说法不正确的是( )| A. | 在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2CrO42-+2H+?Cr2O72-+H2O向右移动 | |
| B. | 在阴极室,通电后KOH溶液不断变浓,并产生气体H2 | |
| C. | CrO42-通过离子交换膜从阳极区域迁移到阴极区域 | |
| D. | 电解一段时间后测定阳极液中K和Cr的物质的量之比为d,则导线中转移电子的物质的量为(2-d)mol |
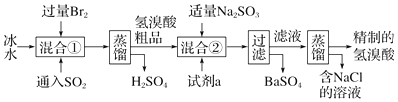
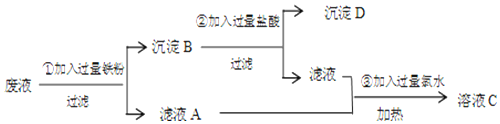
 .
.