13.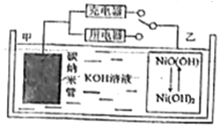 氢燃料电池具有广阔前景.某二次氢燃料电池的原理如图所示,该电池用吸附了H2的碳纳米管等材料制作而成,下列说法正确的是( )
氢燃料电池具有广阔前景.某二次氢燃料电池的原理如图所示,该电池用吸附了H2的碳纳米管等材料制作而成,下列说法正确的是( )
 氢燃料电池具有广阔前景.某二次氢燃料电池的原理如图所示,该电池用吸附了H2的碳纳米管等材料制作而成,下列说法正确的是( )
氢燃料电池具有广阔前景.某二次氢燃料电池的原理如图所示,该电池用吸附了H2的碳纳米管等材料制作而成,下列说法正确的是( )| A. | 放电时,甲电极为正极,OH-移向乙电极 | |
| B. | 可开发氢燃料电池用于电动汽车 | |
| C. | 电池总反应为H2+NiO(OH)$?_{充电}^{放电}$Ni(OH)2 | |
| D. | 充电时,乙电极反应式为NiO(OH)+H2O+e-=Ni(OH)2+OH- |
12.下列有关物质的性质与用途都正确且具有对应关系的是( )
| A. | NH4HCO3受热易分解,可用作氮肥 | |
| B. | Na2CO3具有碱性,可用作胃酸中和剂 | |
| C. | SiO2易传导光信号,可用作光导纤维 | |
| D. | Ca(ClO)2在空气中不稳定,可用于漂白纸张 |
11.下列有关化学用语表示正确的是( )
| A. | 中子数为20的氯原子:${\;}_{17}^{20}$Cl | B. | S2-的结构示意图: | ||
| C. | CaO2的电子式: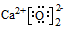 | D. | 葡萄糖的结构简式:C6H12O6 |
10.有3.92g铁的氧化物,用足量的CO在高温下将其还原,把生成的全部CO2通入到足量的澄清的石灰水中得到7.0g固体沉淀物,这种铁的氧化物为( )
| A. | Fe3O4 | B. | FeO | C. | Fe2O3 | D. | Fe5O7 |
9.下列褪色与二氧化硫漂白性有关的是( )
| A. | 溴水 | B. | 品红溶液 | ||
| C. | 酸性高锰酸钾溶液 | D. | 滴入酚酞的氢氧化钠溶液 |
8.下列符合元素周期律的是( )
| A. | 碱性:Ca(OH)2>Mg(OH)2 | B. | 酸性:H2SO3>H2CO3 | ||
| C. | 热稳定性:NH3<PH3 | D. | 还原性:S2-<Cl- |
7.元素①~⑩在周期表中的位置如表所示,试回答下列问题.
(1)上述10种元素中,化学性质最不活泼的是Ar(填元素符号,下同);与水反应最激烈的金属元素是K.
(2)元素 ②的气态氢化物的分子式是NH3;上述10种元素中,其最高价氧化物对应水化物的酸性最强的物质是HClO4(填化学式).
(3)用电子式表示元素③与④形成1:2型化合物的形成过程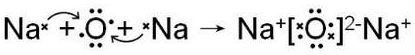 .
.
(4)①②⑤元素的原子半径由小到大的顺序为N、C、Mg(用元素符号表示);③⑦⑩元素的气态氢化物的稳定性由强到弱的顺序为H2O、HCl、HBr(用氢化物的化学式表示).
(5)④和⑥两元素的最高价氧化物对应的水化物相互反应的离子方程式:Al(OH)3+OH-═AlO2-+2H2O.
周期 族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)元素 ②的气态氢化物的分子式是NH3;上述10种元素中,其最高价氧化物对应水化物的酸性最强的物质是HClO4(填化学式).
(3)用电子式表示元素③与④形成1:2型化合物的形成过程
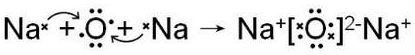 .
.(4)①②⑤元素的原子半径由小到大的顺序为N、C、Mg(用元素符号表示);③⑦⑩元素的气态氢化物的稳定性由强到弱的顺序为H2O、HCl、HBr(用氢化物的化学式表示).
(5)④和⑥两元素的最高价氧化物对应的水化物相互反应的离子方程式:Al(OH)3+OH-═AlO2-+2H2O.
5.能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.
(1)工业上合成甲醇的反应原理为:CO(g)+2H2(g)?CH3OH(g)△H;下表所列数据是该反应在不同温度下的化学平衡常数(K).
①写出该反应的平衡常数表达式K=$\frac{c(C{H}_{3}OH)}{c(CO)•{c}^{2}({H}_{2})}$.
②下列措施可以加快反应速率且能提高CO转化率的是c.
a.再充入CO b.将甲醇液化并及时分离出c.增大压强 d.加入催化剂 e.降低温度
③在300℃时,将2molCO、3mol H2和2mol CH3OH充入容积为1L的密闭容器中,此时反应将向正反应方向进行 (填“向正反应方向进行”“向逆反应方向进行”或“处于平衡状态”).
(2)以甲醇、氧气为原料,KOH溶液作为电解质构成燃料电池总反应为:2CH3OH+3O2+4OH-=2CO32-+6H2O,则负极的电极反应式为:CH3OH+8OH--6e-=CO32-+6H2O.
(3)如果以该燃料电池为电源,石墨作两极电解饱和食盐水,则该电解过程中阳极的电极反应式为:2Cl--2e-=Cl2↑;如果电解一段时间后NaC1溶液的体积为1L,溶液中的OH-物质的量浓度为0.01mol•L-1(25℃下测定),则理论上消耗氧气的体积为56mL(标况下).
(1)工业上合成甲醇的反应原理为:CO(g)+2H2(g)?CH3OH(g)△H;下表所列数据是该反应在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②下列措施可以加快反应速率且能提高CO转化率的是c.
a.再充入CO b.将甲醇液化并及时分离出c.增大压强 d.加入催化剂 e.降低温度
③在300℃时,将2molCO、3mol H2和2mol CH3OH充入容积为1L的密闭容器中,此时反应将向正反应方向进行 (填“向正反应方向进行”“向逆反应方向进行”或“处于平衡状态”).
(2)以甲醇、氧气为原料,KOH溶液作为电解质构成燃料电池总反应为:2CH3OH+3O2+4OH-=2CO32-+6H2O,则负极的电极反应式为:CH3OH+8OH--6e-=CO32-+6H2O.
(3)如果以该燃料电池为电源,石墨作两极电解饱和食盐水,则该电解过程中阳极的电极反应式为:2Cl--2e-=Cl2↑;如果电解一段时间后NaC1溶液的体积为1L,溶液中的OH-物质的量浓度为0.01mol•L-1(25℃下测定),则理论上消耗氧气的体积为56mL(标况下).
4.在甲乙丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同):N2(g)+3H2(g)?2NH3(g)△H<0,相关数据如表所示:下列说法正确的是( )
0 162842 162850 162856 162860 162866 162868 162872 162878 162880 162886 162892 162896 162898 162902 162908 162910 162916 162920 162922 162926 162928 162932 162934 162936 162937 162938 162940 162941 162942 162944 162946 162950 162952 162956 162958 162962 162968 162970 162976 162980 162982 162986 162992 162998 163000 163006 163010 163012 163018 163022 163028 163036 203614
| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | lmol N2、3molH2 | 2mol NH3 | 2mol NH3 |
| 平衡时容器体积 | V甲 | V乙 | V丙 |
| 反应的平衡常数K | K甲 | K乙 | K丙 |
| 平衡时NH3的浓度/mol•L-1 | C甲 | C乙 | C丙 |
| 平衡时NH3的反应速率/mol•L-1•min-1 | v甲 | V乙 | V丙 |
| A. | V甲>V丙 | B. | C乙>C甲 | C. | K乙>K丙 | D. | V甲=V丙 |
 为保护环境,应减少二氧化硫、氮氧化物和二氧化碳等物质的排放量.
为保护环境,应减少二氧化硫、氮氧化物和二氧化碳等物质的排放量.