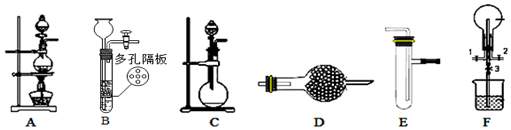
18.下列关于化学与生活的一些说法中不正确的是( )
| A. | 卤水点豆腐、明矾净水的原理都是破坏胶体的介稳性 | |
| B. | 铁、铝、铜制容器放置空气中都能在表面形成致密氧化物 | |
| C. | 单晶Ge是半导体,可以作为光电转换材料用于太阳能电池 | |
| D. | 检测酒后驾车者呼出气中的乙醇属于化学检测方法 |
17.下列“化学知识原理”对“实际应用”的解释说明错误的是( )
| 选项 | 实际应用 | 化学知识原理 |
| A | 选用金属锂做锂电池的负极 | 锂轻且在空气中稳定 |
| B | 工业采用高压(20-50MPa)合成NH3 | 应用勒夏特列原理 |
| C | 施加石膏降低盐碱地(含Na2CO3)的碱性 | CaCO3溶度积小于CaSO4 |
| D | 在船身上装锌块来避免船体遭受腐蚀 | Zn比Fe活泼 |
| A. | A | B. | B | C. | C | D. | D |
16.下列与化学有关说法中正确的是( )
| A. | ${\;}_{53}^{127}$I和${\;}_{53}^{131}$I2互为同位素 | |
| B. | lmol碳酸钾晶体中含阴离子数为等于NA个 | |
| C. | 分子式为C4H8O2的羧酸共有3种 | |
| D. | 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-=3Fe3++NO↑+3H2O |
15.下列有关说法不正确的是( )
| A. | 反应SiO2(s)+3C(s)═SiC(s)+2CO(g)室温下不能自发进行,则该反应的△H>0 | |
| B. | 等pH的CH3COOH、HCl溶液混合后,平衡不移动,但c(CH3COO-)减少 | |
| C. | 配制KF溶液时,必需要加入KOH溶液抑制F-水解 | |
| D. | 向NaHS溶液中滴入少量CuCl2溶液产生黑色沉淀,HS-电离程度增大,pH减小 |
14.化学实验安全处理不正确的是( )
| A. | 苯酚沾在皮肤上用大量水冲洗 | |
| B. | 金属钠着火时,立即用沙子盖灭 | |
| C. | 制备氯气时,应用NaOH溶液吸收多余的氯气 | |
| D. | 制备乙烯时向乙醇和浓硫酸的混合液中加碎瓷片 |
13.如图是元素周期表的一部分
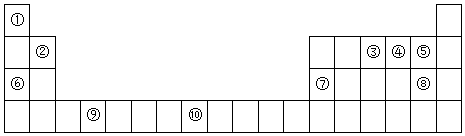
(1)元素⑩原子结构示意图为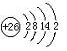 .
.
(2)元素 ③④⑤的电负性由大到小的顺序为F>O>N(填化学用语,下同),其简单离子半径由大到小的顺序为N3->O2->F-.⑤与⑧气态氢化物中稳定性较强的是HF.
(3)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的单质及其化合物有相似的性质.写出元素②的最高价氧化物与NaOH溶液反应的离子方程式2OH-+BeO=BeO22-+H2O
(4)根据下列五种元素的第一至第四电离能数据(单位:KJ•mol-1),回答下面各题:
①在周期表中,最可能处于同一主族的是R和U.(填元素代号)
②T元素最可能是p(填“s”、“p”、“d”、“ds”等)区元素;若T为第二周期元素,Z是第三周期元素中原子半径最小的主族元素,则T、Z形成的化合物分子键角为120°.
(5)金刚砂(SiC)的结构与金刚石相似,硬度与金刚石相当,则金刚砂的晶胞中含有4个硅原子,4个碳原子,其中硅原子的杂化方式为sp3.

(1)元素⑩原子结构示意图为
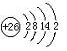 .
.(2)元素 ③④⑤的电负性由大到小的顺序为F>O>N(填化学用语,下同),其简单离子半径由大到小的顺序为N3->O2->F-.⑤与⑧气态氢化物中稳定性较强的是HF.
(3)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的单质及其化合物有相似的性质.写出元素②的最高价氧化物与NaOH溶液反应的离子方程式2OH-+BeO=BeO22-+H2O
(4)根据下列五种元素的第一至第四电离能数据(单位:KJ•mol-1),回答下面各题:
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
②T元素最可能是p(填“s”、“p”、“d”、“ds”等)区元素;若T为第二周期元素,Z是第三周期元素中原子半径最小的主族元素,则T、Z形成的化合物分子键角为120°.
(5)金刚砂(SiC)的结构与金刚石相似,硬度与金刚石相当,则金刚砂的晶胞中含有4个硅原子,4个碳原子,其中硅原子的杂化方式为sp3.
11.某化学反应2A?B+D在三种不同条件下进行,B、D的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如表所示,表中温度为摄氏度(℃).
根据上述数据,回答下列问题:
(1)在实验1中,以反应物A浓度的变化表示该反应在0~10min内的平均反应速率为0.02mol/(L•min)
(2)在实验1中,c1数值为0.50
(3)在实验1、2中有一个实验使用了正催化剂.判断是实验2 (选填“1”或“2”)使用了正催化剂.
(4)在实验1、3中反应温度不同.判断T3> 800(选填“<”或“>”).
| 实验 序号 | 浓度 时间 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | c1 | 0.50 |
| 2 | 800 | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | T3 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)在实验1中,以反应物A浓度的变化表示该反应在0~10min内的平均反应速率为0.02mol/(L•min)
(2)在实验1中,c1数值为0.50
(3)在实验1、2中有一个实验使用了正催化剂.判断是实验2 (选填“1”或“2”)使用了正催化剂.
(4)在实验1、3中反应温度不同.判断T3> 800(选填“<”或“>”).
10.为了研究外界条件对H2O2分解速率的影响,有同学利用实验室提供的仪器和试剂设计了如下4组实验.注意:设计实验时,必须控制只有一个变量!
试剂:4% H2O2溶液,12% H2O2溶液,lmol/LFeCl3溶液
仪器:试管、带刻度的胶头滴管、酒精灯
(1)甲同学为了研究温度对化学反应速率的影响,应完成1、2实验(填组别).
(2)乙同学进行实验3与实验4,发现气体均缓慢产生,无法说明“浓度改变会影响化学反应速率”,你的改进方法是再同时分别向试管甲和试管乙中滴加2~3滴lmol/LFeCl3溶液作为催化剂.
(3)丙同学进行了实验1与实验4,你认为他想探究的是探究催化剂对化学反应速率的影响.该方案设计是否严谨?否(填是或否),说明理由试管中加入1mL1mol/LFeCl3溶液会使H2O2溶液的浓度降低.
试剂:4% H2O2溶液,12% H2O2溶液,lmol/LFeCl3溶液
仪器:试管、带刻度的胶头滴管、酒精灯
| 组别 | 实验温度 (℃) | H2O2溶液 | FeCl3溶液 (1mol/L) |
| 1 | 30 | 5mL 4% | 1mL |
| 2 | 60 | 5mL 4% | 1mL |
| 3 | 30 | 5mL 12% | |
| 4 | 30 | 5mL 4% |
(2)乙同学进行实验3与实验4,发现气体均缓慢产生,无法说明“浓度改变会影响化学反应速率”,你的改进方法是再同时分别向试管甲和试管乙中滴加2~3滴lmol/LFeCl3溶液作为催化剂.
(3)丙同学进行了实验1与实验4,你认为他想探究的是探究催化剂对化学反应速率的影响.该方案设计是否严谨?否(填是或否),说明理由试管中加入1mL1mol/LFeCl3溶液会使H2O2溶液的浓度降低.
9.下列有关化学用语说法正确的( )
0 162826 162834 162840 162844 162850 162852 162856 162862 162864 162870 162876 162880 162882 162886 162892 162894 162900 162904 162906 162910 162912 162916 162918 162920 162921 162922 162924 162925 162926 162928 162930 162934 162936 162940 162942 162946 162952 162954 162960 162964 162966 162970 162976 162982 162984 162990 162994 162996 163002 163006 163012 163020 203614
| A. | 过氧化氢的电子式: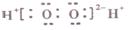 | |
| B. | 比例模型  既可以表示甲烷分子,也可以表示四氯化碳分子 既可以表示甲烷分子,也可以表示四氯化碳分子 | |
| C. | 次氯酸的结构式H-O-Cl | |
| D. | 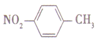 表示对硝基甲苯的结构简式 表示对硝基甲苯的结构简式 |