6.下列实验操作不能达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 制备乙炔时,减缓乙炔的生成速率 | 用饱和食盐水替代水跟电石反应 |
| B | 证明NH4Cl溶液能促进Mg(OH)2固体的溶解 | 向两份等量的Mg(OH)2固体中分别加入等体积的蒸馏水和NH4Cl溶液 |
| C | 验证乙醇发生消去反应生成乙烯 | 将生成的气体直接通入含Br2的CCl4溶液中 |
| D | 证明Al2O3的熔点比Al高 | 把砂纸打磨过的铝箔在酒精灯上加热至熔化 |
| A. | A | B. | B | C. | C | D. | D |
5.下列说法中正确的是( )
| A. | 分子中键能越大,键长越长,则分子越稳定 | |
| B. | 乳酸分子[CH3-CH(OH)-COOH]中有 1 个手性碳且 1 mol 该分子中有 11 mol σ 键 | |
| C. | PCl5分子中P原子和Cl原子最外层都满足8电子结构 | |
| D. | H-O键键能为463 kJ/mol,即18 g H2O分解成H2和O2时,消耗能量为2×463 kJ |
20.氯元素在自然界有35Cl和37Cl两种同位素,在计算式34.969×75.77%+36.966×24.23%=35.453中( )
| A. | 75.77%表示35Cl的质量分数 | |
| B. | 24.23%表示35Cl在自然界所占的原子个数百分比 | |
| C. | 35.453表示氯元素的相对原子质量 | |
| D. | 36.966表示37Cl的质量数 |
18.为探究元素性质递变规律,设计如下实验.
(1)填写各实验步骤对应的实验现象(选填相应序号;不重复选).
A.剧烈反应,迅速产生大量无色气体.
B.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色.
C.反应不十分剧烈;产生无色气体.
D.有气体产生,溶液变成浅红色.
(2)实验④:向1mL 1mol/L AlCl3溶液中滴加2mol/L NaOH溶液至过量,观察生成白色胶状沉淀,继而沉淀消失.
请用离子方程式解释该实验现象:Al3++3OH-═Al(OH)3↓;、Al(OH)3+OH-═AlO2-+2H2O
(3)实验⑤:在试管中加入3~5mL Na2SiO3溶液,逐滴加入稀硫酸,边加边振荡.观察试管中出现白色凝胶.相应化学方程式:H2SO4+Na2SiO3═H2SiO3(胶体)+Na2SiO4,证明酸性:H2SO4>H2SiO3(用化学式表示).
(4)实验⑥:向新制得的Na2S溶液中滴加新制的氯水.观察试管中出现黄色沉淀.相应离子方程式:S2-+Cl2═S↓+2Cl-,证明氧化性:Cl2>S(用化学式表示).
通过以上实验和讨论,推断钠、镁、铝的金属性逐渐减弱 (选填“增强”或“减弱”),硅、硫、氯的非金属性逐渐增强(选填“增强”或“减弱”).
(1)填写各实验步骤对应的实验现象(选填相应序号;不重复选).
| 实验序号 | 实验步骤 | 实验现象 |
| ① | 将一小块金属钠放入滴有酚酞溶液的冷水中. | B |
| ② | 将磨去表面氧化膜的一小段镁条放入试管中,加入2mL水,滴入2滴酚酞溶液,加热至水沸腾. | D |
| ③ | 将磨去表面氧化膜的一小段镁条投入2mL 1mol/L盐酸中. | A |
| ④ | 将磨去表面氧化膜的一小片铝投入2mL 1mol/L盐酸中. | C |
B.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色.
C.反应不十分剧烈;产生无色气体.
D.有气体产生,溶液变成浅红色.
(2)实验④:向1mL 1mol/L AlCl3溶液中滴加2mol/L NaOH溶液至过量,观察生成白色胶状沉淀,继而沉淀消失.
请用离子方程式解释该实验现象:Al3++3OH-═Al(OH)3↓;、Al(OH)3+OH-═AlO2-+2H2O
(3)实验⑤:在试管中加入3~5mL Na2SiO3溶液,逐滴加入稀硫酸,边加边振荡.观察试管中出现白色凝胶.相应化学方程式:H2SO4+Na2SiO3═H2SiO3(胶体)+Na2SiO4,证明酸性:H2SO4>H2SiO3(用化学式表示).
(4)实验⑥:向新制得的Na2S溶液中滴加新制的氯水.观察试管中出现黄色沉淀.相应离子方程式:S2-+Cl2═S↓+2Cl-,证明氧化性:Cl2>S(用化学式表示).
通过以上实验和讨论,推断钠、镁、铝的金属性逐渐减弱 (选填“增强”或“减弱”),硅、硫、氯的非金属性逐渐增强(选填“增强”或“减弱”).
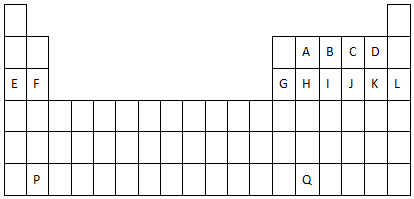
17.元素周期律表明( )
0 162816 162824 162830 162834 162840 162842 162846 162852 162854 162860 162866 162870 162872 162876 162882 162884 162890 162894 162896 162900 162902 162906 162908 162910 162911 162912 162914 162915 162916 162918 162920 162924 162926 162930 162932 162936 162942 162944 162950 162954 162956 162960 162966 162972 162974 162980 162984 162986 162992 162996 163002 163010 203614
| A. | 随着原子序数的增大,元素的主要化合价逐渐增加 | |
| B. | 随着随着相对原子质量的增大,元素的化学性质会不断重复 | |
| C. | 与碱金属相比,其相邻主族的(碱土)金属具有更小的密度和硬度 | |
| D. | 卤素氢化物的稳定性随着核电荷数的增加而减弱 |
 ;
;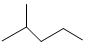 表示的分子式C6H14;系统命名法的名称是2-甲基戊烷.
表示的分子式C6H14;系统命名法的名称是2-甲基戊烷.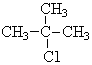 .
.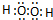 .
. ,用电子式表示A2C的形成过程.
,用电子式表示A2C的形成过程.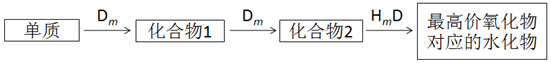
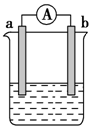 如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:
如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题: