1.X、Y、Z、Q、R是五种短周期元素,原子序数依次增大,部分元素在周期表中的位置关系如右图所示.其中X是周期表中原子半径最小的元素,Q与X同主族;Z的最外层电子数是次外层的3倍.
请回答下列问题:
(1)写出Y元素的名称:氮,Q的原子结构示意图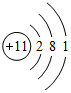 ;R在周期表中的位置为第三周期ⅢA族.
;R在周期表中的位置为第三周期ⅢA族.
(2)Q2Z电子式为: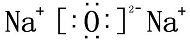 ,Q2Z2含的化学键类型为:离子键、共价键.
,Q2Z2含的化学键类型为:离子键、共价键.
(3)R、Z分别形成简单离子的半径大小:Al3+<O2-(离子符号表示)
(4)Y的氢化物与其最高价氧化物对应的水化物反应的化学方程式为:NH3+HNO3═NH4NO3.
| Y | Z | ||
| R |
(1)写出Y元素的名称:氮,Q的原子结构示意图
 ;R在周期表中的位置为第三周期ⅢA族.
;R在周期表中的位置为第三周期ⅢA族.(2)Q2Z电子式为:
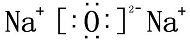 ,Q2Z2含的化学键类型为:离子键、共价键.
,Q2Z2含的化学键类型为:离子键、共价键.(3)R、Z分别形成简单离子的半径大小:Al3+<O2-(离子符号表示)
(4)Y的氢化物与其最高价氧化物对应的水化物反应的化学方程式为:NH3+HNO3═NH4NO3.
20.镁铝合金5.1g溶于500mL 1mol/L的盐酸中,向反应后的溶液中加入过量 NaOH溶液,最终生成5.8g白色沉淀.下列有关说法不正确的是( )
| A. | 白色沉淀为Mg(OH)2 | |
| B. | 在加入NaOH过程中生成沉淀最多为13.6g | |
| C. | 生成H2体积为5.6L | |
| D. | 刚加NaOH 溶液就有沉淀生成 |
19.将少量的铝投入过量的氢氧化钠溶液中充分反应,下列有关所得混合溶液的叙述正确的是( )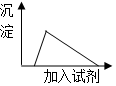

| A. | 该溶液中,Ag+、K+、NH4+、SO42-可以大量共存 | |
| B. | 该溶液中,Na+、OH-、NO3-、CO32-不能大量共存 | |
| C. | 向该溶液中逐滴加入AlCl3溶液,生成沉淀与加入AlCl3溶液关系如图 | |
| D. | 向该溶液中逐滴加入稀盐酸,生成沉淀与加入稀盐酸关系如图 |
18.要将SiO2 固体中Al2O3杂质除去,可用的试剂是( )
| A. | 浓氨水 | B. | NaOH溶液 | C. | 盐酸 | D. | CO2和水 |
17.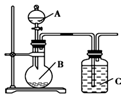 某研究性学习小组根据元素非金属性与其最高价氧化物对应的水化物之间的关系,设计了如图装置来一次性完成S、C、Si的非金属性强弱比较的实验研究,下列关于试剂B选择正确的是( )
某研究性学习小组根据元素非金属性与其最高价氧化物对应的水化物之间的关系,设计了如图装置来一次性完成S、C、Si的非金属性强弱比较的实验研究,下列关于试剂B选择正确的是( )
 某研究性学习小组根据元素非金属性与其最高价氧化物对应的水化物之间的关系,设计了如图装置来一次性完成S、C、Si的非金属性强弱比较的实验研究,下列关于试剂B选择正确的是( )
某研究性学习小组根据元素非金属性与其最高价氧化物对应的水化物之间的关系,设计了如图装置来一次性完成S、C、Si的非金属性强弱比较的实验研究,下列关于试剂B选择正确的是( )| A. | 稀H2SO4 | B. | Na2SO4溶液 | C. | Na2CO3溶液 | D. | Na2SiO3溶液 |
15.化学与生产、生活、社会密切相关,下列有关说法不正确的是( )
| A. | “地沟油”可以制成肥皂,提高资源的利用率 | |
| B. | 为防止食品氧化变质,常在食品包装袋中放入生石灰 | |
| C. | 用加热灼烧的方法可以区分羊毛毛线和腈纶毛线 | |
| D. | 加快开发髙效洁净能源转换技术,缓解能源危机 |
14.下列实验设计及其对应的离子方程式均正确的是( )
| A. | 工业制漂白粉:C12+2OH-═Cl-+ClO-+H2O | |
| B. | 将氯气溶于水制备次氯酸:C12+H2O═2H++Cl-+ClO- | |
| C. | 用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+═Cu2++2Fe2+ | |
| D. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O |
13.下列说法正确的是( )
0 162800 162808 162814 162818 162824 162826 162830 162836 162838 162844 162850 162854 162856 162860 162866 162868 162874 162878 162880 162884 162886 162890 162892 162894 162895 162896 162898 162899 162900 162902 162904 162908 162910 162914 162916 162920 162926 162928 162934 162938 162940 162944 162950 162956 162958 162964 162968 162970 162976 162980 162986 162994 203614
| A. | 保护钢铁水闸门可用外接电源阳极保护法 | |
| B. | 反应NH3(g)+HI(g)═NH4I(s)在低温下可自发进行,则△H>0,△S>0 | |
| C. | 常温下,向0.lmol•L-1CH3COONa溶液中滴加盐酸,溶液中水的电离程度增大 | |
| D. | 恒温下进行的反应2NO2(g)?N2O4(g)达平衡时,缩小容器体积再达平衡时,气体 的颜色比第一次平衡时的深 |
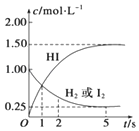 698K时,向某V L的密闭容器中充入3mol H2(g)和3mol I2(g),发生反应:H2(g)+I2(g)?2HI(g),测得各物质的物质的量浓度与时间变化的关系如右图所示.请回答下列问题:
698K时,向某V L的密闭容器中充入3mol H2(g)和3mol I2(g),发生反应:H2(g)+I2(g)?2HI(g),测得各物质的物质的量浓度与时间变化的关系如右图所示.请回答下列问题: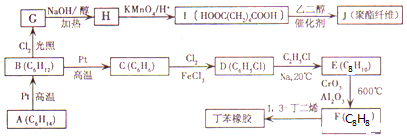
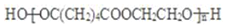 .
.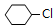 +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$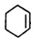 +NaCl+H2O.
+NaCl+H2O.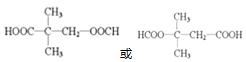 (写出其中一种的结构简式).
(写出其中一种的结构简式).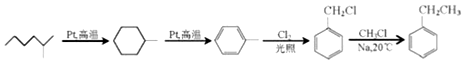 .
.