10.把Ca(OH)2固体放入一定量的蒸馏水中,一定温度下达到平衡:Ca(OH)2(s)?Ca2+(aq)+2OH-(aq).当向悬浊液中加少量生石灰后,若温度保持不变,下列判断正确的是( )
| A. | 溶液中Ca2+数目减少 | B. | 溶液pH值增大 | ||
| C. | 溶液中c(Ca2+)增大 | D. | 溶液pH值不变 |
9.已知:Ksp[Mg(OH)2]=1.8×10-11 Ksp[Zn(OH)2]=1.0×10-17
Ksp[Cr(OH)3]=7.0×10-31 Ksp[Fe(OH)3]=4.0×10-38
若将浓度均为0.01mol/L的Fe3+、Cr3+、Zn2+、Mg2+四种离子组成溶液的pH控制在9附近,溶液中四种离子的浓度由大到小排列顺序正确是( )
Ksp[Cr(OH)3]=7.0×10-31 Ksp[Fe(OH)3]=4.0×10-38
若将浓度均为0.01mol/L的Fe3+、Cr3+、Zn2+、Mg2+四种离子组成溶液的pH控制在9附近,溶液中四种离子的浓度由大到小排列顺序正确是( )
| A. | Mg2+、Zn2+、Cr3+、Fe3+ | B. | Cr3+、Fe3+、Zn2+、Mg2+ | ||
| C. | Fe3+、Cr3+、Zn2+、Mg2+ | D. | Zn2+、Mg2+、Cr3+、Fe3+ |
5.真空碳热还原-氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
①Al2O3(s)+3C(s)=2Al(s)+3CO(g)△H1=1344.1kJ•mol-1
②2AlCl3(g)=2Al(s)+3Cl2(g)△H2=1169.2kJ•mol-1
③Al2O3(s)+3C(s)+3Cl2(g)=2AlCl3(g)+3CO(g)△H3=Q kJ•mol-1
下列有关说法正确的是( )
①Al2O3(s)+3C(s)=2Al(s)+3CO(g)△H1=1344.1kJ•mol-1
②2AlCl3(g)=2Al(s)+3Cl2(g)△H2=1169.2kJ•mol-1
③Al2O3(s)+3C(s)+3Cl2(g)=2AlCl3(g)+3CO(g)△H3=Q kJ•mol-1
下列有关说法正确的是( )
| A. | 反应①中化学能转化为热能 | |
| B. | 反应②中若生成液态铝则反应热应大于△H2 | |
| C. | 反应③中1molAlCl3(g)生成时,需要吸收174.9kJ的热量 | |
| D. | 该生产工艺中能循环利用的物质只有AlCl3 |
3.某酸性工业废水中含有Ag+、Cu2+、Pb2+等重金属离子,化工生产中常用FeS作为沉淀剂去除它们,其中除Cu2+的反应原理为Cu2+(aq)+FeS(s)?CuS(s)+Fe2+(aq).下列有关说法正确的是( )
0 162789 162797 162803 162807 162813 162815 162819 162825 162827 162833 162839 162843 162845 162849 162855 162857 162863 162867 162869 162873 162875 162879 162881 162883 162884 162885 162887 162888 162889 162891 162893 162897 162899 162903 162905 162909 162915 162917 162923 162927 162929 162933 162939 162945 162947 162953 162957 162959 162965 162969 162975 162983 203614
| A. | 若c(Fe2+)与c(Cu2+)相等时,该反应达到平衡状态 | |
| B. | 向平衡体系中加入少量硫酸铜晶体后,FeS的KSP减小 | |
| C. | 其他条件不变,增大FeS的物质的量,该反应的正反应速率增大 | |
| D. | 该反应的化学平衡常数K=$\frac{{K}_{sp}(FeS)}{{K}_{sp}(CuS)}$ |
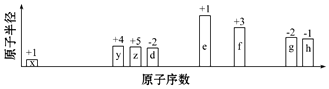
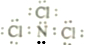 .
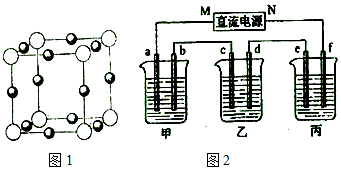
.
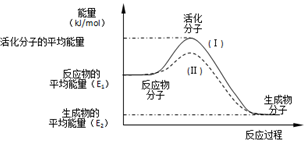 在化学反应中,只有极少数分子的能量比所有分子的平均能量高得多,只有这些高能量的分子发生碰撞时才可能发生化学反应,人们把这些高能量的分子称为活化分子,其他分子成为普通分子.把活化分子的平均能量与反应物分子的平均能量之间的差值叫活化能,单位为kJ/mol.请认真观察如图后回答问题.
在化学反应中,只有极少数分子的能量比所有分子的平均能量高得多,只有这些高能量的分子发生碰撞时才可能发生化学反应,人们把这些高能量的分子称为活化分子,其他分子成为普通分子.把活化分子的平均能量与反应物分子的平均能量之间的差值叫活化能,单位为kJ/mol.请认真观察如图后回答问题.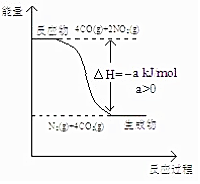 研究 NOx、SO2、CO 等大气污染气体的处理具有重要意义.
研究 NOx、SO2、CO 等大气污染气体的处理具有重要意义.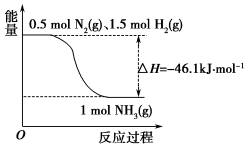 氨在工农业生产中应用广泛.
氨在工农业生产中应用广泛.