17.下列变化中,不需要破坏化学键的是( )
| A. | HCl溶于水 | B. | 食盐熔融 | C. | 碘单质溶于苯 | D. | 石油裂化 |
16.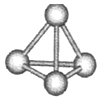 意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂lmolN-N吸收167kJ热量,生成1mol N≡N放出945kJ热量.根据以上信息和数据,下列说法正确的是( )
意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂lmolN-N吸收167kJ热量,生成1mol N≡N放出945kJ热量.根据以上信息和数据,下列说法正确的是( )
 意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂lmolN-N吸收167kJ热量,生成1mol N≡N放出945kJ热量.根据以上信息和数据,下列说法正确的是( )
意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂lmolN-N吸收167kJ热量,生成1mol N≡N放出945kJ热量.根据以上信息和数据,下列说法正确的是( )| A. | N4属于由非极性键构成的极性分子 | |
| B. | 氮元素非金属性比磷强,可知N4沸点比P4(白磷)高 | |
| C. | lmol N4气体转变为N2气体放出888kJ热量 | |
| D. | N4与N2互为同位素 |
15.已知CuO高温灼烧生成Cu2O,Cu2O与稀H2SO4反应的离子方程式:Cu2O+2H+═Cu+Cu2++H2O.现将经高温灼烧后的CuO样品投入足量稀硫酸中得到混合溶液,有关说法正确的是( )
| A. | 反应中Cu2O只作氧化剂 | |
| B. | 若有28.8g Cu2O参加反应,则转移电子数为0.2NA | |
| C. | Cu2O的稳定性比CuO弱 | |
| D. | 如果溶液中出现蓝色,说明CuO已分解 |
14.下列有关叙述能说明非金属元素M比N的非金属性强的是( )
| A. | 非金属单质M能从N的化合物中置换出非金属单质N | |
| B. | 在反应中M原子比N原子得到更多电子 | |
| C. | M的气态氢化物稳定性比N弱 | |
| D. | M的氧化物对应水化物的酸性比N强 |
13.取一定质量的铜片和一定体积的浓硫酸放在烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,若要使铜片继续溶解可向烧瓶中加入( )
| A. | 稀H2SO4 | B. | 稀盐酸 | C. | K2SO4固体 | D. | KNO3固体 |
12.下列离子反应方程式正确的是( )
| A. | 少量二氧化碳通入“水玻璃”中:CO2+SiO32-+H2O═CO32-+H2SiO3↓ | |
| B. | 碳酸钙与稀盐酸混合:CO32-+2H+═CO2↑+H2O | |
| C. | 铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ | |
| D. | Al2O3溶于NaOH溶液中:Al2O3+2OH-═2[Al(OH)4]- |
11.可逆反应N2+3H2$?_{催化剂}^{高温高压}$2NH3,在体积不变的密闭容器中反应,达到平衡状态的标志是( )
| A. | 单位时间内生成n molN2的同时生成n molNH3 | |
| B. | N2、H2、NH3的物质的量浓度比值为1:3:2 | |
| C. | v(N2)=v(NH3) | |
| D. | 单位时间内断裂1mol氮氮键的同时断裂6mol氮氢键 |
10.对于100mL1mol/L盐酸与铁片的反应,采取下列措施,其中不能使反应速率加快的是( )
| A. | 升高温度 | B. | 改用50mL2mol/L盐酸 | ||
| C. | 改用200mL1mol/L盐酸 | D. | 用等量铁粉代替铁片 |
9.下列有关说法正确的是( )
| A. | NaOH是只含离子键的离子化合物 | |
| B. | HCl溶于水没有破坏共价键 | |
| C. | 碳在O2中燃烧时,破坏碳和O2中化学键吸收的总能量大于形成CO2中化学键释放的总能量 | |
| D. | 在Cl2+2NaBr=2NaCl+Br2反应过程中有离子键和共价键的断裂,也有离子键和共价键形成 |
8.铷元素(Rb)位于元素周期表中第五周期第ⅠA族,有关Rb及其化合物的性质推测正确的是( )
0 162779 162787 162793 162797 162803 162805 162809 162815 162817 162823 162829 162833 162835 162839 162845 162847 162853 162857 162859 162863 162865 162869 162871 162873 162874 162875 162877 162878 162879 162881 162883 162887 162889 162893 162895 162899 162905 162907 162913 162917 162919 162923 162929 162935 162937 162943 162947 162949 162955 162959 162965 162973 203614
| A. | Rb与冷水反应比K更剧烈 | B. | Rb投入CuSO4溶液中可置换出Cu | ||
| C. | Rb与O2反应只有Rb2O产生 | D. | Rb2CO3难溶于水 |