7.X2-离子核外有a个电子,b个中子,则该微粒X原子可表示为( )
| A. | a+b+2a+2 X | B. | a+b-2a-2 X | C. | b-2a+2 X | D. | ba X |
6.下列反应中,不属于可逆反应的是( )
| A. | Cl2与水反应 | |
| B. | 水电解生成H2 和H2在O2中燃烧生成水的相互转化过程 | |
| C. | 工业合成氨 | |
| D. | 氨气与水反应 |
5.下列反应过程中的能量变化与如图相符的是( )


| A. | 金属钠和水反应 | B. | 生石灰变成熟石灰的反应 | ||
| C. | Al和Fe2O3的铝热反应 | D. | CaCO3受热分解 |
4.下列物质中属于共价化合物的是( )
| A. | NH4Cl | B. | CuSO4 | C. | CO2 | D. | Br2 |
3.下列说法中,正确的是( )
| A. | 二氧化硅可用来制造太阳能电池 | |
| B. | 需要加热才能进行的反应一定是吸热反应 | |
| C. | 铜的金属性比铝弱,可以用铜罐贮运浓硝酸 | |
| D. | NaOH溶液不能保存在带磨口玻璃塞的试剂瓶中 |
2.NH3作为一种重要化工原料,被大量应用于工业生产,与其有关性质反应的 催化剂研究催化剂常具有较强的选择性,即专一性.已知:
反应 I:4NH3(g)+5O2(g)$\stackrel{PtRu}{?}$4NO(g)+6H2O(g)△H=-905.0kJ•mol-1
反应 II:4NH3(g)+3O2(g)$?_{高温}^{CU/TiO_{2}}$2N2(g)+6H2O(g)△H
(1)
△H=-1260KJ/mol.
(2)在恒温恒容装置中充入一定量的 NH3 和 O2,在某催化剂的作用下进行反应 I,则下 列有关叙述中正确的是A.
A.使用催化剂时,可降低该反应的活化能,加快其反应速率
B.若测得容器内 4v 正(NH3)=6v 逆(H2O)时,说明反应已达平衡
C.当容器内 $\frac{n(NO)}{n(N{H}_{3})}$=1 时,说明反应已达平衡
(3)氨催化氧化时会发生上述两个竞争反应 I、II.为分析某催化剂对该反应的选择性,在 1L 密闭容器中充入 1mol NH3和 2mol O2,测得有关物质的量关系如图:
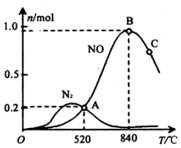
①该催化剂在高温时选择反应I(填“I”或“II”).
②520℃时,4NH3(g)+5O2?4NO(g)+6H2O(g)的平衡常数K=$\frac{0.{2}^{4}×0.{9}^{6}}{0.{4}^{4}×1.4{5}^{5}}$(不要求得出计算结果,只需列出数字计算式).
③有利于提高 NH3 转化为 N2 平衡转化率的措施有E
A.使用催化剂 Pt/Ru
B.使用催化剂 Cu/TiO2
C.增大 NH3和 O2 的初始投料比
D.投料比不变,增加反应物的浓度
E.降低反应温度
(4)采用氨水吸收烟气中的 SO2,
①若氨水与 SO2恰好完全反应生成正盐,则此时溶液呈碱性(填“酸”或“碱”). 常温下弱电解质的电离平衡常数如下:氨水:Kb=1.8×10-5mol•L-1;H2SO3:Ka1=1.3×10-2mol•L-1,Ka2=6.3×10-8mol•L-1
②上述溶液中通入SO2(填“SO2”或 NH3”)气体可使溶液呈中性,此时溶液中$\frac{c{(NH}_{4}^{+})}{c(S{{O}_{3}}^{2-})}$>2(填“>”“<”或“=”)
反应 I:4NH3(g)+5O2(g)$\stackrel{PtRu}{?}$4NO(g)+6H2O(g)△H=-905.0kJ•mol-1
反应 II:4NH3(g)+3O2(g)$?_{高温}^{CU/TiO_{2}}$2N2(g)+6H2O(g)△H
(1)
| 化学键 | H-O | O=O | N≡N | N-H |
| 键能KJ•mol-1 | 463 | 496 | 942 | 391 |
(2)在恒温恒容装置中充入一定量的 NH3 和 O2,在某催化剂的作用下进行反应 I,则下 列有关叙述中正确的是A.
A.使用催化剂时,可降低该反应的活化能,加快其反应速率
B.若测得容器内 4v 正(NH3)=6v 逆(H2O)时,说明反应已达平衡
C.当容器内 $\frac{n(NO)}{n(N{H}_{3})}$=1 时,说明反应已达平衡
(3)氨催化氧化时会发生上述两个竞争反应 I、II.为分析某催化剂对该反应的选择性,在 1L 密闭容器中充入 1mol NH3和 2mol O2,测得有关物质的量关系如图:

①该催化剂在高温时选择反应I(填“I”或“II”).
②520℃时,4NH3(g)+5O2?4NO(g)+6H2O(g)的平衡常数K=$\frac{0.{2}^{4}×0.{9}^{6}}{0.{4}^{4}×1.4{5}^{5}}$(不要求得出计算结果,只需列出数字计算式).
③有利于提高 NH3 转化为 N2 平衡转化率的措施有E
A.使用催化剂 Pt/Ru
B.使用催化剂 Cu/TiO2
C.增大 NH3和 O2 的初始投料比
D.投料比不变,增加反应物的浓度
E.降低反应温度
(4)采用氨水吸收烟气中的 SO2,
①若氨水与 SO2恰好完全反应生成正盐,则此时溶液呈碱性(填“酸”或“碱”). 常温下弱电解质的电离平衡常数如下:氨水:Kb=1.8×10-5mol•L-1;H2SO3:Ka1=1.3×10-2mol•L-1,Ka2=6.3×10-8mol•L-1
②上述溶液中通入SO2(填“SO2”或 NH3”)气体可使溶液呈中性,此时溶液中$\frac{c{(NH}_{4}^{+})}{c(S{{O}_{3}}^{2-})}$>2(填“>”“<”或“=”)
1.下列溶液中氢离子浓度最小的是( )
| A. | 10L0.10mol/LCH3COOH 溶液 | B. | 2L 0.05mol/L H2SO4溶液 | ||
| C. | lL0.10mol/LHNO3溶液 | D. | 2L0.1mol/LHCl溶液 |
20.配制一定物质的量浓度的Na2CO3溶液时,下下列因素会导致溶液浓度偏高的是( )
| A. | 溶解时有少量液体溅出 | B. | 洗涤液未全部转移到容量瓶中 | ||
| C. | 容量瓶使用前未干燥 | D. | 定容时液面未到刻度线 |
19.下列物质的分离方法的原理与溶解度不相关的是( )
| A. | 蒸馏分馏 | B. | 重结晶法 | C. | 纸层析法 | D. | 萃取分液 |
18.下列各式表示水解反应的是( )
0 162778 162786 162792 162796 162802 162804 162808 162814 162816 162822 162828 162832 162834 162838 162844 162846 162852 162856 162858 162862 162864 162868 162870 162872 162873 162874 162876 162877 162878 162880 162882 162886 162888 162892 162894 162898 162904 162906 162912 162916 162918 162922 162928 162934 162936 162942 162946 162948 162954 162958 162964 162972 203614
| A. | HCO3-+H2O?H3O++CO32- | B. | HS-+H2O?H2S+OH- | ||
| C. | HSO3-+H2O?SO32-+H3O+ | D. | HCO3-+OH-?H2O+CO32- |