3.下列转化中,碳原子间的连接形式未发生改变的是( )
| A. | 丁酮的催化加氢反应 | B. | 丙酮与HCN发生加成反应 | ||
| C. | 乙醛与乙醛反应生成2-羟基丁醛 | D. | 乙苯与酸性高锰酸钾溶液反应 |
2.X、Y、Z、W四种常见元素,其中X、Y、Z为短周期元素,W为过渡元素,它们的相关信息如表:
回答下列问题:
(1)W在周期表的位置为第四周期第Ⅷ族,W(OH)2在空气中不稳定,极易被氧化反应的化学方程式为4Fe(OH)2+O2+2H2O═4Fe(OH)3.
(2)X的简单阴离子的结构示意图为 ;X的最高价氧化物对应水化物的水溶液与Y的氧化物反应的离子方程式为6H++Al2O3=2Al3++3H2O.
;X的最高价氧化物对应水化物的水溶液与Y的氧化物反应的离子方程式为6H++Al2O3=2Al3++3H2O.
(3)Z的氧化物在通讯领域的用途是光导纤维,工业上制备Z的单质的化学反应方程式为Ge+2 H2O2+2NaOH=Na2GeO3+3H2O.
(4)YX3固体在熔融状态下不导电,则YX3固体中存在共价键;在50mL l mol•L-1的YX3溶液中逐滴加入0.5mol•L-1的NaOH溶液,得到1.56g沉淀,则加入NaOH溶液的体积可能有二种情况.
| 原子或分子相关信息 | 单质及其化合物相关信息 | |
| X | ZX4分子是由粗Z提纯Z的中间产物 | X的最高价氧化物对应的水化物为无机酸中最强酸 |
| Y | Y原子的最外层电子数等于电子层数 | Y的氧化物是典型的两性氧化物,可用于制造一种高温材料 |
| Z | Z原子的最外层电子数是次外层电子数的$\frac{1}{2}$ | Z广泛存在于无机非金属材料中,其单质是制取大规模集成电路的主要原料 |
| W | W原子的最外层电子数小于4 | W的常见化合价有+3、+2,WX3稀溶液呈黄色 |
(1)W在周期表的位置为第四周期第Ⅷ族,W(OH)2在空气中不稳定,极易被氧化反应的化学方程式为4Fe(OH)2+O2+2H2O═4Fe(OH)3.
(2)X的简单阴离子的结构示意图为
 ;X的最高价氧化物对应水化物的水溶液与Y的氧化物反应的离子方程式为6H++Al2O3=2Al3++3H2O.
;X的最高价氧化物对应水化物的水溶液与Y的氧化物反应的离子方程式为6H++Al2O3=2Al3++3H2O.(3)Z的氧化物在通讯领域的用途是光导纤维,工业上制备Z的单质的化学反应方程式为Ge+2 H2O2+2NaOH=Na2GeO3+3H2O.
(4)YX3固体在熔融状态下不导电,则YX3固体中存在共价键;在50mL l mol•L-1的YX3溶液中逐滴加入0.5mol•L-1的NaOH溶液,得到1.56g沉淀,则加入NaOH溶液的体积可能有二种情况.
1.下列有关化学用语表示正确的是( )
| A. | 次氯酸的结构式:H-Cl-O | B. | 1H、2H、3H是同一种核素 | ||
| C. | S2-的结构示意图: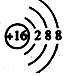 | D. | 四氯化碳的电子式: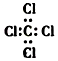 |
20.下列实验操作可以达到目的是( )
| 目的 | 操作 | |
| A | 提纯含有少量乙酸的乙酸乙酯 | 向含有少量乙酸的乙酸乙酯中加入过量饱和碳酸钠溶液,振荡后静置分液,并除去有机相的水 |
| B | 检验溴乙烷中的溴元素 | 取样,加NaOH溶液,振荡后再加AgNO3溶液 |
| C | 提纯含有少量苯酚的苯 | 向含有少量苯酚的苯中加入过量的浓溴水振荡后静置过滤,除去三溴苯酚沉淀 |
| D | 检验蔗糖是否水解 | 蔗糖溶液在稀硫酸存在下水浴加热一段时间后,再与银氨溶液混合加热,观察现象 |
| A. | A | B. | B | C. | C | D. | D |
19.下列关于有机化合物的说法正确的是( )
| A. | 聚氯乙烯分子中含碳碳双键 | B. | 乙醇、苯和溴苯用水即可鉴别 | ||
| C. | 汽油、柴油、植物油都是碳氢化合物 | D. | 油脂的皂化反应属于加成反应 |
17.下列关于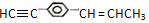 的说法正确的是( )
的说法正确的是( )
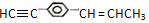 的说法正确的是( )
的说法正确的是( )| A. | 所有碳原子有可能都在同一平面上 | |
| B. | 最多只可能有9个碳原子在同一平面上 | |
| C. | 有7个碳原子可能在同一直线上 | |
| D. | 至少有6个碳原子在同一直线上 |
16.按要求填写下列空白:
(1)将10molA 和smolB 充入SL 密闭容器中,某温度下发生反应:3A+B?2C ( A、B、C均为气体),在最初2s内,v(A)为0.6mol/(L•s).则在2s时,B的物质的量浓度为0.6mol/L,C 的体积分数为$\frac{0.8S}{10-S}$×100%(小数点后保留一位).
(2)某同学为了探究锌与盐酸反应过程中的速率变化,他在100mL1.0mol/L盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气(气体体积已折算为标准状况),实验记录如表(累计值)
①哪一时间段(0-1min、1-2min、2-3min、3-4min、4-5min)反应速率最慢4~5min,原因是因为4~5min时H+浓度小(或酸的浓度小).
②求2-3min时间段内以盐酸的浓度变化表示的该反应的反应速率0.1mol/(L•min)(忽略溶液体积的变化).
③为了减缓反应速率而又不减少产生氢气的量,该同学在盐酸中分别加入等体积的下列}溶液:
A.蒸馏水 B.NaCl溶液 C.0.5mol/L盐酸
你认为可行的是(填序号)ABC.
(1)将10molA 和smolB 充入SL 密闭容器中,某温度下发生反应:3A+B?2C ( A、B、C均为气体),在最初2s内,v(A)为0.6mol/(L•s).则在2s时,B的物质的量浓度为0.6mol/L,C 的体积分数为$\frac{0.8S}{10-S}$×100%(小数点后保留一位).
(2)某同学为了探究锌与盐酸反应过程中的速率变化,他在100mL1.0mol/L盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气(气体体积已折算为标准状况),实验记录如表(累计值)
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL | 50 | 120 | 232 | 290 | 310 |
②求2-3min时间段内以盐酸的浓度变化表示的该反应的反应速率0.1mol/(L•min)(忽略溶液体积的变化).
③为了减缓反应速率而又不减少产生氢气的量,该同学在盐酸中分别加入等体积的下列}溶液:
A.蒸馏水 B.NaCl溶液 C.0.5mol/L盐酸
你认为可行的是(填序号)ABC.
15.表列出了元素周期表中6种短周期元素的有关数据.
根据表中信息回答下列问题(均使用化学用语填空):
(1)写出下列编号对应元素的符号:②P,③Li.
(2)表中元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质反应生成的盐的化学式为NaClO4.
(3)请写出①、②、④三种元素的简单氢化物的稳定性由强到弱的顺序HF>NH3>PH3.
(4)元素⑥所在的主族中,氢化物的还原性最强的是HI.
(放射性元素除外)
0 162709 162717 162723 162727 162733 162735 162739 162745 162747 162753 162759 162763 162765 162769 162775 162777 162783 162787 162789 162793 162795 162799 162801 162803 162804 162805 162807 162808 162809 162811 162813 162817 162819 162823 162825 162829 162835 162837 162843 162847 162849 162853 162859 162865 162867 162873 162877 162879 162885 162889 162895 162903 203614
| 元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 原子半径(nm) | 0.075 | 0.110 | 0.152 | 0.071 | 0.186 | 0.099 |
| 最高价态 | +5 | +5 | +1 | 0 | +1 | +7 |
| 最低价态 | -3 | -3 | 0 | -1 | 0 | -1 |
(1)写出下列编号对应元素的符号:②P,③Li.
(2)表中元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质反应生成的盐的化学式为NaClO4.
(3)请写出①、②、④三种元素的简单氢化物的稳定性由强到弱的顺序HF>NH3>PH3.
(4)元素⑥所在的主族中,氢化物的还原性最强的是HI.
(放射性元素除外)
 酚酞是白色结晶,在空气中稳定,几乎不溶于水,常用做酸碱指示剂,其结构简式如图:
酚酞是白色结晶,在空气中稳定,几乎不溶于水,常用做酸碱指示剂,其结构简式如图: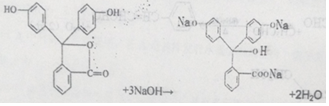 .
.