2. 氢是一种清洁的可再生能源.
氢是一种清洁的可再生能源.
(1)已知:
若1g水蒸气变为液态水时放出2.4KJ热量,则表示氢气燃烧热的热化学方程式为H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.2kJ/mol.
(2)氢的稳定存储是氢能源发展的关键.固态合金具有较强的吸附氢原子能力,其原理可表示为(以M代表固态合金):2M(s)+xH2(g) $?_{释放}^{存储}$2MHx(s)△H<0
①有利于氢气存储的条件为低温,高压;
②该反应的平衡常数的表达式为$K=\frac{1}{{{c^x}({H_2})}}$;
③达平衡后保持恒温恒压下增加氢气的量,该平衡向右移动(填“向左”、“向右”、或“不”)
(3)储氢合金可做二次电池的电极,其工作原理为:xNi(OH)2+M$?_{放电}^{充电}$MHx+xNiOOH.装置如图所示:
①a为电源的负极;
②写出充电时阴极反应式xH2O+xe-+M=MHx+xOH-;
③以该电池做电源电解饱和NaCl溶液,当手机到标准状况下11.2LH2时,储氢合金理论上释放出1g氢,此时有1molOH-由B向A(填“A”或“B”)移动.
 氢是一种清洁的可再生能源.
氢是一种清洁的可再生能源.(1)已知:
| 化学键 | H-H(g) | H-O(g) | O≡O(g) |
| 键能(KJ/mol) | 436 | 463 | 496 |
(2)氢的稳定存储是氢能源发展的关键.固态合金具有较强的吸附氢原子能力,其原理可表示为(以M代表固态合金):2M(s)+xH2(g) $?_{释放}^{存储}$2MHx(s)△H<0
①有利于氢气存储的条件为低温,高压;
②该反应的平衡常数的表达式为$K=\frac{1}{{{c^x}({H_2})}}$;
③达平衡后保持恒温恒压下增加氢气的量,该平衡向右移动(填“向左”、“向右”、或“不”)
(3)储氢合金可做二次电池的电极,其工作原理为:xNi(OH)2+M$?_{放电}^{充电}$MHx+xNiOOH.装置如图所示:
①a为电源的负极;
②写出充电时阴极反应式xH2O+xe-+M=MHx+xOH-;
③以该电池做电源电解饱和NaCl溶液,当手机到标准状况下11.2LH2时,储氢合金理论上释放出1g氢,此时有1molOH-由B向A(填“A”或“B”)移动.
20.下列各组物质中,一定属于同系物的是( )
0 162699 162707 162713 162717 162723 162725 162729 162735 162737 162743 162749 162753 162755 162759 162765 162767 162773 162777 162779 162783 162785 162789 162791 162793 162794 162795 162797 162798 162799 162801 162803 162807 162809 162813 162815 162819 162825 162827 162833 162837 162839 162843 162849 162855 162857 162863 162867 162869 162875 162879 162885 162893 203614
| A. | 乙二醇和丙三醇 | B. | C6H5OH和C6H5CH2OH | ||
| C. | C3H6和C4H8 | D. | C3H8和C4H10 |
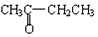
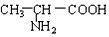 与
与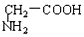
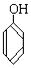 和
和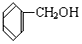
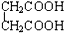 和
和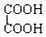
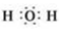 .
.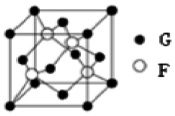 A、B、C、D、E、F、G七种元素位于元素周期表前四周期,原子序数依次增大.元素周期表中原子半径最小的是A,B原子最外层有两个未成对电子,化合物CD2为红棕色气体,E的单质易与水反应且只作氧化剂,元素F基态原子的3p轨道上有5个电子,G是第四周期元素,最外层只有一个电子,其余各层电子均充满.
A、B、C、D、E、F、G七种元素位于元素周期表前四周期,原子序数依次增大.元素周期表中原子半径最小的是A,B原子最外层有两个未成对电子,化合物CD2为红棕色气体,E的单质易与水反应且只作氧化剂,元素F基态原子的3p轨道上有5个电子,G是第四周期元素,最外层只有一个电子,其余各层电子均充满.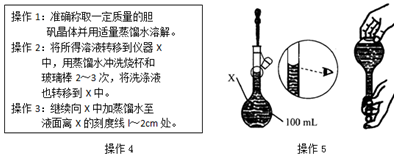
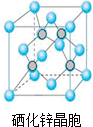 (1)基态硒原子的价层电子排布式为4s24p4.
(1)基态硒原子的价层电子排布式为4s24p4.