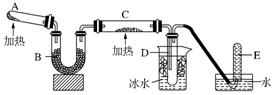
12.从键长的角度来判断下列共价键中最稳定的是( )
| A. | H-F | B. | H-N | C. | H-C | D. | H-S |
9.下列化合物中,既有离子键又有共价键的离子化合物是( )
| A. | NH4Cl | B. | MgO | C. | HNO3 | D. | CaCl2 |
8.下列关于离子键、共价键的叙述中正确的是( )
| A. | 非极性键只存在于双原子的单质分子(如Cl2)中 | |
| B. | 在共价化合物里,可能存在离子键 | |
| C. | 在离子化合物里,只存在离子键,没有共价键 | |
| D. | 化学反应的实质是旧键的断裂,新键的形成 |
7.下列各组物质及粒子性质变化不正确的是( )
| A. | 氧化性:F2>Cl2 | B. | 碱性:Mg(OH)2>Al(OH)3 | ||
| C. | 金属单质置换出氢的能力:K>Na | D. | 酸性:H2SO4>HClO4 |
6.Na+、Mg2+、F-、O2-四种离子具有相同的电子层结构.则四种元素原子半径由大到小的顺序分别是( )
| A. | Mg>Na>F>O | B. | O>F>Na>Mg | C. | Na>Mg>O>F | D. | O>F>Na>Mg |
5.表是某城市空气质量每周公报的部分内容.下列选项中不会对表中3个空气质量指标产生影响的是( )
| 项目 | 空气污染指数(API) | 空气质量级别 | 空气质量描述 |
| 总悬浮颗粒 | 52 | Ⅱ | 良 |
| 二氧化硫 | 7 | I | 优 |
| 二氧化氮 | 24 | I | 优 |
| A. | 用煤和石油产品作燃料 | B. | 汽车排放的尾气 | ||
| C. | 使用含磷洗衣粉 | D. | 焚烧垃圾 |
4.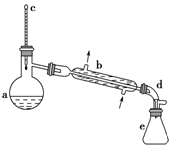 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:
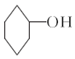 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$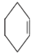 +H2O,
+H2O,
可能用到的有关数据如表:
合成反应:
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓H2SO4,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯12g.
回答下列问题:
(1)装置b的名称是直形冷凝管(或冷凝管).
(2)本实验中最容易产生的副产物的结构简式为 ,生成该物质的反应类型是取代反应
,生成该物质的反应类型是取代反应
(3)分液漏斗在使用前须清洗干净并检漏,在本实验分离过程中,产物应该从分液漏斗的上口倒出(填“上口倒出”或“下口倒出”).
(4)在环己烯粗产物蒸馏过程中,不可能用到的仪器有CE(填正确答案标号).
A.蒸馏烧瓶 B.温度计 C.分液漏斗D.锥形瓶 E.蒸发皿
(5)本实验所得到的环己烯产率是73.2%.
 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图: $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O,
+H2O,可能用到的有关数据如表:
| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.961 8 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.810 2 | 83 | 难溶于水 |
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓H2SO4,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯12g.
回答下列问题:
(1)装置b的名称是直形冷凝管(或冷凝管).
(2)本实验中最容易产生的副产物的结构简式为
 ,生成该物质的反应类型是取代反应
,生成该物质的反应类型是取代反应(3)分液漏斗在使用前须清洗干净并检漏,在本实验分离过程中,产物应该从分液漏斗的上口倒出(填“上口倒出”或“下口倒出”).
(4)在环己烯粗产物蒸馏过程中,不可能用到的仪器有CE(填正确答案标号).
A.蒸馏烧瓶 B.温度计 C.分液漏斗D.锥形瓶 E.蒸发皿
(5)本实验所得到的环己烯产率是73.2%.
3.设NA为阿伏加德罗常数的值,下列说法中不正确的是( )
0 162691 162699 162705 162709 162715 162717 162721 162727 162729 162735 162741 162745 162747 162751 162757 162759 162765 162769 162771 162775 162777 162781 162783 162785 162786 162787 162789 162790 162791 162793 162795 162799 162801 162805 162807 162811 162817 162819 162825 162829 162831 162835 162841 162847 162849 162855 162859 162861 162867 162871 162877 162885 203614
| A. | 1molC2H4Cl2中含有共用电子对数目为7NA | |
| B. | 标准状况下,44.8 L丙三醇与足量金属钠反应,生成气体的分子数为3NA | |
| C. | 20℃时,1 mol己烷完全燃烧后恢复至原状态,生成气态物质分子数为6NA | |
| D. | 15g甲基正离子(CH3+)所含有的电子数是8NA |