15.下列指定反应的离子方程式正确的是( )
| A. | 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3 NH4+ | |
| B. | 向FeI2溶液中加入少量氯水:2 Fe2++Cl2═2Fe3++2Cl-(已知:2Fe3++2I-═2 Fe2++I2) | |
| C. | 将过量铁粉投入稀硝酸中:3Fe+8H++2NO3-═3Fe3++2NO↑+4H2O | |
| D. | 将SO2通入Na2O2粉末中的主要反应为:2Na2O2+2SO2═2 Na2SO3+O2 |
14.设阿伏加德罗常数的数值为N A,下列说法不正确的是( )
| A. | 加热条件下足量的铜粉与含0.2 mol H2SO4的浓硫酸充分反应,转移电子数目为0.2 NA | |
| B. | 0.1 mol CaO2中含有的阴、阳离子总数为0.2 NA | |
| C. | 1.6 g CH4中含有的C-H键数目为0.4 NA | |
| D. | 标准状况下,2.24 L H37Cl含有的中子数为2.0 NA |
13.氢化钠NaH是一种白色的离子晶体,其中钠是+1价.NaH与水反应放出氢气.下列叙述中,正确的是( )
| A. | NaH在水中显酸性 | |
| B. | NaH中氢离子半径比锂离子半径大 | |
| C. | NaH中氢离子可被还原为氢气 | |
| D. | Na与其它碱金属都必须保存在煤油中 |
12.为实现实验目的,选用的装置、实验操作均正确的是( )
| 实验目的 | 实验步骤和装置 | |
| A | 验证SO2具有漂白性 | 将SO2通入氢氧化钠的酚酞试液中 |
| B | 探究温度对反应速率的影响 | 不同温度下,取0.1 mol/LKI 溶液,向其中先加入淀粉溶液,再加入0.1 mol/L 硫酸,记录溶液出现蓝色的时间 |
| C | 验证牺牲阳极的阴极保护法 | 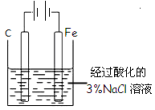 往铁电极附近滴加铁氰化钾溶液 |
| D | 检验蔗糖水解产物具有还原性 | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,再向其中加入新制的Cu(OH)2,加热3-5min. |
| A. | A | B. | B | C. | C | D. | D |
11.有机物M是合成某药品的中间体,结构简式如图所示.下列说法错误的是( )


| A. | M能发生酯化、加成、氧化反应 | |
| B. | 用碳酸氢钠不能检验M分子中存在羧基 | |
| C. | M的分子式为C8H8O4 | |
| D. | M的苯环上一氯代物有2种 |
10.下列金属冶炼的反应原理,错误的是( )
| A. | 2NaCl(熔融)$\stackrel{通电}{→}$ 2Na+Cl2↑ | B. | MgO+H2$\stackrel{△}{→}$Mg+H2O | ||
| C. | Fe3O4+4CO3$\stackrel{高温}{→}$Fe+4CO2 | D. | 2HgO 2$\stackrel{△}{→}$Hg+O2↑ |
9.下列物质不能通过化合反应制得的是( )
| A. | FeCl2 | B. | NaHCO3 | C. | Al(OH)3 | D. | Fe(OH)3 |
8.下列反应的离子反应方程式正确的是( )
0 162636 162644 162650 162654 162660 162662 162666 162672 162674 162680 162686 162690 162692 162696 162702 162704 162710 162714 162716 162720 162722 162726 162728 162730 162731 162732 162734 162735 162736 162738 162740 162744 162746 162750 162752 162756 162762 162764 162770 162774 162776 162780 162786 162792 162794 162800 162804 162806 162812 162816 162822 162830 203614
| A. | 过量的二氧化碳通入NaOH溶液中:CO2+OH-═HCO3- | |
| B. | 氯气通入水中:Cl2+H2O═Cl-+ClO-+2H+ | |
| C. | 硫酸亚铁溶液加入过氧化氢溶液 Fe2++2H2O2+4H+═Fe3++4H2O | |
| D. | 向AlCl3溶液中过量的氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |