10.下列热化学方程式正确的是( )
| A. | 甲烷的燃烧热为890.3KJ•mol-1,则甲烷燃烧热的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30 MPa 下,将0.1 mol N2 和 0.3 mol H2 置于密闭容器中充分反应生成NH3(g),放热3.86 KJ,其热化学方程式为:N2(g)+3H2(g)$?_{500℃30MPa}^{催化剂}$ 2NH3(g)△H=-38.6 KJ•mol-1 | |
| C. | 已知1 g液态肼和足量液态过氧化氢反应生成氮气和水蒸气时放出20.05 kJ的热量,肼和过氧化氢反应的热化学方程式为: N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.6 KJ•mol-1 | |
| D. | CO(g)的燃烧热是283.0 KJ•mol-1,则2CO2(g)═2CO(g)+O2(g) 反应的△H=+283.0 KJ•mol-1 |
9.根据图,下列判断中正确的是( )
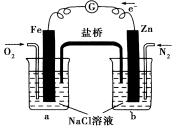

| A. | 烧杯b中发生还原反应 | |
| B. | 烧杯b中发生的反应为2Cl--2e-═Cl2↑ | |
| C. | 烧杯a中发生的反应为2H++2e-═H2↑ | |
| D. | 烧杯a中的溶液pH升高 |
7.一定条件下,向2L恒容密闭容器中充入1mol PCl5,发生反应:PCl5(g)?PCl3(g)+Cl2(g)
反应过程中测定的部分数据见表(反应过程中条件不变):
请回答下列问题:
(1)x 的值是0.2;
(2)0-50s 内,用PCl3的浓度变化表示的化学反应速率是0.0016mol/(L•s);
(3)250s 以后,Cl2的物质的量不再改变的原因是250s达到平衡,正逆反应速率相等,条件不变,各组分的物质的量都不再变化;
(4)250s 时,容器中Cl2的物质的量是0.2mol,PCl5的物质的量是0.8mol,PCl5的转化率是20%.
反应过程中测定的部分数据见表(反应过程中条件不变):
| t/s | 0 | 30 | 150 | 250 | 350 | 450 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 | x |
(1)x 的值是0.2;
(2)0-50s 内,用PCl3的浓度变化表示的化学反应速率是0.0016mol/(L•s);
(3)250s 以后,Cl2的物质的量不再改变的原因是250s达到平衡,正逆反应速率相等,条件不变,各组分的物质的量都不再变化;
(4)250s 时,容器中Cl2的物质的量是0.2mol,PCl5的物质的量是0.8mol,PCl5的转化率是20%.
4.某同学做同周期元素性质递交规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表:
请你帮助该同学整理并完成实验报告
(1)实验目的:验证同周期元素金属性、非金属性的变化规律.
(2)实验用品:略.
(3)实验内容:(填写题给信息表中相应的实验现象,并在有空格处写出相对应的离子方程式)
(4)实验结论:同周期元素随原子序数的增大,元素的金属性逐渐减弱,而非金属性逐渐增强.
(5)问题与讨论:
请从原子结构理论上简单说明具有上述结论的原因是同周期元素随核电荷数的增加,原子核对核外电子的束缚力增强,原子半径减小,原子失电子能力减弱,而得到电子能力增强,即元素金属性逐渐减弱,二非金属性逐渐增强.
| 实验方案 | 实验现象 |
| ①用砂纸打磨后的镁带与沸水反应;再向反应液中滴加酚酞 | 产生气体,气体可燃,溶液变浅红色 |
| ②向新制得Na2S饱和溶液中滴加新制氯水 | 生成淡黄色沉淀 |
| ③钠与滴有酚酞试液的冷水反应 | 浮于水面上,熔成小球,四处游动,逐渐缩小,溶液变红色 |
| ④镁带与2mol/L的盐酸反应 | 剧烈反应,产生的气体可燃 |
| ⑤铝条与2mol/L的盐酸反应 | 反应不十分剧烈;产生的气体可燃 |
| ⑥向AlCl3溶液中滴加NaOH溶液至过量 | 先生成白色絮状沉淀,最后沉淀全部溶解 |
| 实验方案 | 实验现象 | 有关离子方程式 |
| ① | 不填 | 不填 |
| ② | S2-+Cl2=S↓+2Cl- | |
| ③ | 不填 | 2Na+2H2O=2Na++2OH-+H2↑ |
| ④ | 不填 | 不填 |
| ⑤ | 不填 | 2Al+6H+=2Al3++3H2↑ |
| ⑥ | 先生成白色絮状沉淀,最后沉淀全部溶解 | Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=AlO2-+2H2O |
(2)实验用品:略.
(3)实验内容:(填写题给信息表中相应的实验现象,并在有空格处写出相对应的离子方程式)
(4)实验结论:同周期元素随原子序数的增大,元素的金属性逐渐减弱,而非金属性逐渐增强.
(5)问题与讨论:
请从原子结构理论上简单说明具有上述结论的原因是同周期元素随核电荷数的增加,原子核对核外电子的束缚力增强,原子半径减小,原子失电子能力减弱,而得到电子能力增强,即元素金属性逐渐减弱,二非金属性逐渐增强.
3.不能说明X的非金属性比Y强的是( )
| A. | X单质可以把Y从其氢化物中置换出来 | |
| B. | X的最高价氧化物的水化物的酸性比Y的最高价氧化物的水化物的酸性强 | |
| C. | 与H2化合时X单质比Y单质容易 | |
| D. | X原子的最外层电子数比Y原子的最外层电子数多 |
2.下列两种物质发生反应:①Na和O2②A1Cl3与氨水 ③水玻璃与CO2 ④Fe与Cl2⑤Fe和稀HNO3,因反应物用量或反应条件的不同而生成不同产物的是( )
| A. | ①②③④⑤ | B. | ①③⑤ | C. | ①②③⑤ | D. | ①②⑤ |
1.下列说法中不正确的是( )
0 162588 162596 162602 162606 162612 162614 162618 162624 162626 162632 162638 162642 162644 162648 162654 162656 162662 162666 162668 162672 162674 162678 162680 162682 162683 162684 162686 162687 162688 162690 162692 162696 162698 162702 162704 162708 162714 162716 162722 162726 162728 162732 162738 162744 162746 162752 162756 162758 162764 162768 162774 162782 203614
| A. | 光导纤维做通讯材料有许多优点,但怕腐蚀,铺设也很不方便 | |
| B. | 新型无机非金属材料具有光学特性、生物功能、电学特性、耐高温、强度高 | |
| C. | 高温结构陶瓷比金属材料具有许多优点,如耐高温不怕氧化、密度小等优点 | |
| D. | 光导纤维除用于通信外,还可以用于医疗、信息处理等许多方面 |
