9.下列实验操作正确且能达到相应实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 称取2.0g NaOH固体 | 先在左、右两托盘上各放一张滤纸,然后在有盘上添加2g砝码,左盘上添加NaOH固体 |
| B | 检验试液巾是否含有NH4+ | 取少量试液于试管巾,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 |
| C | 除去CO2中混有的杂质SO2 | 将混合气体通入盛有澄清石灰水的洗气瓶中 |
| D | 验证金属钠比铜活泼 | 将钠加入1.0mol•L-1的CuSO4溶液中 |
| A. | A | B. | B | C. | C | D. | D |
8.下列各组微粒具有相同的质子数和电子数的是( )
| A. | OH-、H2O | B. | NH3、NH4+ | C. | H3O+、NH2- | D. | HC1、H2S |
7.下列反应的离子方程式书写正确的是( )
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 将过量氨水加入AlCl3溶液中:Al3++4OH-═AlO2-+2H2O | |
| C. | 酸性溶液中KIO3与KI反应生成I2:IO3-+5I-+6H+═3I2+3H2O | |
| D. | 向NaHCO3溶液中加入等物质的量的Ca(OH)2:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
6.设NA为阿伏加德罗常数的数值,下列说法不正确的是( )
| A. | 标准状况下,22.4 LH2O中含有极性键的数目为2NA | |
| B. | 78 g Na2O2中含有的阴离子数为NA | |
| C. | 11 g重水(D218O)中含有的电子数力5NA | |
| D. | 常温常压下,5.6 g铁粉在7.1 g氯气中充分燃烧,转移的电子数为0.2NA |
5.下列说法正确的是( )
| A. | 元素的种类由最外层电子数决定 | |
| B. | 化学键是存在于分子、原子和离子间的作用力 | |
| C. | 原子的种类由原子核内质子数与中子数共同决定 | |
| D. | 化学反应速率可以决定反应的限度 |
4.图中没有涉及到的能量转化形式是( )


| A. | 化学能转化为热能 | B. | 太阳能转化为化学能 | ||
| C. | 势能转化为电能 | D. | 化学能转化为势能 |
3.在如图所示的微粒中,结合电子能力最强的是( )
| A. | 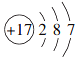 | B. | 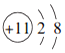 | C. |  | D. |  |
2.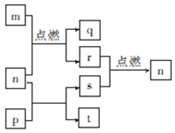 短周期元素W、X、Y、Z的原子序数依次增大,其中Z为金属且Z的原子序数为W的2倍.n、p、q是由这些元素组成的二元化合物,常温下n为气体.m、r、s分别是Z、W、X的单质,t的水溶液显碱性且焰色反应呈黄色,上述物质间的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增大,其中Z为金属且Z的原子序数为W的2倍.n、p、q是由这些元素组成的二元化合物,常温下n为气体.m、r、s分别是Z、W、X的单质,t的水溶液显碱性且焰色反应呈黄色,上述物质间的转化关系如图所示.下列说法正确的是( )
0 162582 162590 162596 162600 162606 162608 162612 162618 162620 162626 162632 162636 162638 162642 162648 162650 162656 162660 162662 162666 162668 162672 162674 162676 162677 162678 162680 162681 162682 162684 162686 162690 162692 162696 162698 162702 162708 162710 162716 162720 162722 162726 162732 162738 162740 162746 162750 162752 162758 162762 162768 162776 203614
 短周期元素W、X、Y、Z的原子序数依次增大,其中Z为金属且Z的原子序数为W的2倍.n、p、q是由这些元素组成的二元化合物,常温下n为气体.m、r、s分别是Z、W、X的单质,t的水溶液显碱性且焰色反应呈黄色,上述物质间的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增大,其中Z为金属且Z的原子序数为W的2倍.n、p、q是由这些元素组成的二元化合物,常温下n为气体.m、r、s分别是Z、W、X的单质,t的水溶液显碱性且焰色反应呈黄色,上述物质间的转化关系如图所示.下列说法正确的是( )| A. | 原子半径:Z>Y | |
| B. | 化合物p中只存在离子键 | |
| C. | 图示转化关系涉及的反应均为氧化还原反应 | |
| D. | 最简单气态氢化物的稳定性:W>X |