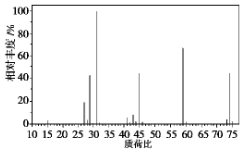
8.三种短周期A、B、C在元素周期表中的位置如表所示.已知A、B、C三种元素的原子最外层电子数之和为15.据此填空:
(1)写出B的元素符号:P,A元素的最高价氧化物的电子式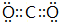 .
.
(2)C元素的某种氢化物可用于实验室中制取O2,其化学式为H2O2.
(3)A元素的某种氢化物是天然气的主要成分,其在光照条件下可以与Cl2发生取代反应,该反应的产物有5种.
(4)写出C的气态氢化物与A的单质反应的化学方程式C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2.
| A | C | |
| B |
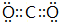 .
.(2)C元素的某种氢化物可用于实验室中制取O2,其化学式为H2O2.
(3)A元素的某种氢化物是天然气的主要成分,其在光照条件下可以与Cl2发生取代反应,该反应的产物有5种.
(4)写出C的气态氢化物与A的单质反应的化学方程式C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2.
5.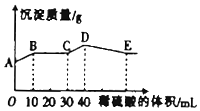 将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解,向混合液中滴加1mol•L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断不正确的是( )
将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解,向混合液中滴加1mol•L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断不正确的是( )
 将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解,向混合液中滴加1mol•L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断不正确的是( )
将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解,向混合液中滴加1mol•L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断不正确的是( )| A. | AB段发生反应的离子方程式为:Ba2++SO42-═BaSO4↓ | |
| B. | E点对应横坐标稀硫酸的体积为70mL | |
| C. | D点表示的沉淀的化学式为Al(OH)3、BaSO4 | |
| D. | E点沉淀比A点沉淀质量大2.33g |
4.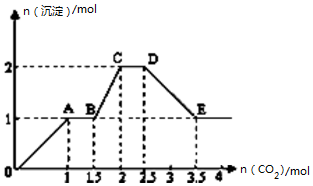 现有易溶强电解质的混合溶液10L,其中可能含存K+、Ba2+、Na+、NH4+、Cl-、SO42-、AlO2-、OH-中的几种,向其中通入CO2气体,产生沉淀的量与通入CO2的量之间的关系如图所示,下列说法正确的是( )
现有易溶强电解质的混合溶液10L,其中可能含存K+、Ba2+、Na+、NH4+、Cl-、SO42-、AlO2-、OH-中的几种,向其中通入CO2气体,产生沉淀的量与通入CO2的量之间的关系如图所示,下列说法正确的是( )
 现有易溶强电解质的混合溶液10L,其中可能含存K+、Ba2+、Na+、NH4+、Cl-、SO42-、AlO2-、OH-中的几种,向其中通入CO2气体,产生沉淀的量与通入CO2的量之间的关系如图所示,下列说法正确的是( )
现有易溶强电解质的混合溶液10L,其中可能含存K+、Ba2+、Na+、NH4+、Cl-、SO42-、AlO2-、OH-中的几种,向其中通入CO2气体,产生沉淀的量与通入CO2的量之间的关系如图所示,下列说法正确的是( )| A. | 该溶液中能确定存在的离子是 Ba2+、AlO2-、NH4+ | |
| B. | 肯定不存在的离子是SO42-、OH- | |
| C. | 若不能确定的离子中至少还存在一种阳离子,则该离子的最小浓度为0.2mol/L | |
| D. | OA 段反应的离子方程式:2 AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
3.SF6是一种优良的绝缘气体,分子结构中只存在S-F键.已知:断裂1mol F-F键、S-F键需吸收的能量分别为160kJ、330kJ.在反应:S(s)+3F2(g)═SF6(g)中,若生成1mol SF6(g)时,放出1220kJ的能量,则1mol S(s)转化为S(g)时吸收的能量为( )
0 162574 162582 162588 162592 162598 162600 162604 162610 162612 162618 162624 162628 162630 162634 162640 162642 162648 162652 162654 162658 162660 162664 162666 162668 162669 162670 162672 162673 162674 162676 162678 162682 162684 162688 162690 162694 162700 162702 162708 162712 162714 162718 162724 162730 162732 162738 162742 162744 162750 162754 162760 162768 203614
| A. | 180 kJ | B. | 220 kJ | C. | 240 kJ | D. | 280 kJ |
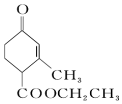 和
和  ,前者不含氧的官能团为(写结构简式)羰基、酯基,后者官能团有(写名称)酯基、羟基;
,前者不含氧的官能团为(写结构简式)羰基、酯基,后者官能团有(写名称)酯基、羟基;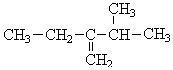 的名称为3-甲基-2-乙基-1-丁烯,
的名称为3-甲基-2-乙基-1-丁烯,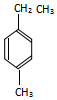 的名称为对甲基乙苯;
的名称为对甲基乙苯;