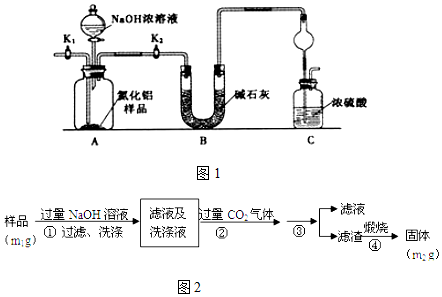
1.某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol•L-1.
甲同学欲探究废水的组成,进行了如下实验:
①用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察).
②取少量溶液,加入KSCN溶液无明显变化.
③另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
④向③中所得的溶液中加入BaCl2溶液,有白色沉淀生成.
请推断:
(1)由①、②、③判断,溶液中一定不含有的阳离子是K+、Fe3+,一定不含的阴离子是CO32-、SiO32-(写离子符号).
(2)③中加入少量盐酸生成无色气体的离子方程式是3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,④中生成白色沉淀的离子方程式是SO42-+Ba2+=BaSO4↓.
(3)将③中所得红棕色气体通入水中,气体变无色,所发生的化学反应方程式为3NO2+H2O=2HNO3+NO.
(4)甲同学最终确定原溶液中所含阳离子是Fe2+、Mg2+,阴离子是Cl-、NO3-、SO42-.(写离子符号)
| 阳离子 | K+ Mg2+ Fe3+ Al3+ Fe2+ |
| 阴离子 | Cl-CO32- NO3- SO42- SiO32- |
①用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察).
②取少量溶液,加入KSCN溶液无明显变化.
③另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
④向③中所得的溶液中加入BaCl2溶液,有白色沉淀生成.
请推断:
(1)由①、②、③判断,溶液中一定不含有的阳离子是K+、Fe3+,一定不含的阴离子是CO32-、SiO32-(写离子符号).
(2)③中加入少量盐酸生成无色气体的离子方程式是3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,④中生成白色沉淀的离子方程式是SO42-+Ba2+=BaSO4↓.
(3)将③中所得红棕色气体通入水中,气体变无色,所发生的化学反应方程式为3NO2+H2O=2HNO3+NO.
(4)甲同学最终确定原溶液中所含阳离子是Fe2+、Mg2+,阴离子是Cl-、NO3-、SO42-.(写离子符号)
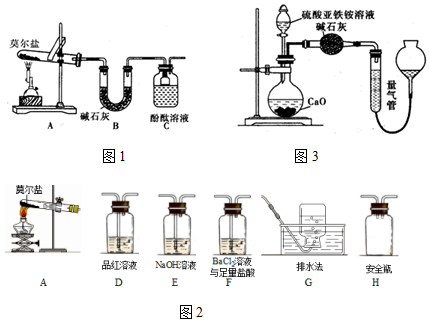
20.某化学研究小组利用如图装置探究FeSO4分解后的产物.
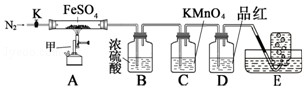
查阅资料得知:SO3溶于水会形成大量的酸雾,工业上通常用浓硫酸做为SO3吸收剂.
实验步骤:按图组装好仪器(已省略夹持仪器)并检查装置的气密性,准确称取m g FeSO4固体置于硬质玻璃管中,将E中的导管撤出水槽,打开活塞K,通入一段时间的N2,关闭活塞K.加热A中的玻璃管一段时间后,将E中导管置于水槽集气瓶口收集产生的气体,用带火星的木条检验E中所收集的气体,带火星的木条能够复燃.待A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却,得到红棕色粉末.请回答下列问题:
(1)B中浓硫酸的作用是吸收分解产生的SO3;
(2)实验前通入一段时间N2,目的是排尽装置中的空气;FeSO4完全分解后,还需要通入一段时间N2,原因是将装置内残留的气体排入吸收装置,使其完全被吸收;
(3)实验过程中发现C中溶液颜色变浅,D中无明显变化.写出C中发生反应的离子方程式5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+;
(4)若C中原先加入了20mL 1.00mol/L的KMnO4溶液,为了确定FeSO4分解的化学方程式,某同学进行了如下实验:
I、称量B装置在实验前后增重0.80g;
II、将实验后C中的溶液全部转移至100mL容量瓶中,并加水稀释至刻度线;
III、准确量取20.00mL溶液至锥形瓶中,加入足量稀硫酸酸化,用0.20mol/L标准H2C2O4溶液滴定至终点;
IV、重复实验3次,记录数据如表
①滴定至终点的现象溶液由紫红色变为无色且半分钟不恢复成紫红色;
②FeSO4分解的化学方程式为8FeSO4$\frac{\underline{\;高温\;}}{\;}$4Fe2O3+2SO3↑+6SO2↑+O2↑;
(5)请设计一个实验来检验A中的FeSO4是否完全分解将废液后的固体转移到小烧杯中,加入少量水搅拌过滤,取少量滤液于试管中,加入几滴K3[Fe(CN)6]溶液,若产生特征蓝色沉淀,说明硫酸亚铁未全部分解,反之则分解完全.

查阅资料得知:SO3溶于水会形成大量的酸雾,工业上通常用浓硫酸做为SO3吸收剂.
实验步骤:按图组装好仪器(已省略夹持仪器)并检查装置的气密性,准确称取m g FeSO4固体置于硬质玻璃管中,将E中的导管撤出水槽,打开活塞K,通入一段时间的N2,关闭活塞K.加热A中的玻璃管一段时间后,将E中导管置于水槽集气瓶口收集产生的气体,用带火星的木条检验E中所收集的气体,带火星的木条能够复燃.待A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却,得到红棕色粉末.请回答下列问题:
(1)B中浓硫酸的作用是吸收分解产生的SO3;
(2)实验前通入一段时间N2,目的是排尽装置中的空气;FeSO4完全分解后,还需要通入一段时间N2,原因是将装置内残留的气体排入吸收装置,使其完全被吸收;
(3)实验过程中发现C中溶液颜色变浅,D中无明显变化.写出C中发生反应的离子方程式5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+;
| 实验 | 滴定管 开始读数 | 滴定 终点读数 |
| 1 | 0 | 19.98 |
| 2 | 0.10 | 20.12 |
| 3 | 0 | 20.16 |
I、称量B装置在实验前后增重0.80g;
II、将实验后C中的溶液全部转移至100mL容量瓶中,并加水稀释至刻度线;
III、准确量取20.00mL溶液至锥形瓶中,加入足量稀硫酸酸化,用0.20mol/L标准H2C2O4溶液滴定至终点;
IV、重复实验3次,记录数据如表
①滴定至终点的现象溶液由紫红色变为无色且半分钟不恢复成紫红色;
②FeSO4分解的化学方程式为8FeSO4$\frac{\underline{\;高温\;}}{\;}$4Fe2O3+2SO3↑+6SO2↑+O2↑;
(5)请设计一个实验来检验A中的FeSO4是否完全分解将废液后的固体转移到小烧杯中,加入少量水搅拌过滤,取少量滤液于试管中,加入几滴K3[Fe(CN)6]溶液,若产生特征蓝色沉淀,说明硫酸亚铁未全部分解,反之则分解完全.
19. 已知在298K和101kPa条件下,有如下反应:
已知在298K和101kPa条件下,有如下反应:
反应Ⅰ:C(s)+O2(g)=CO2(g)△H1=-393.5kJ•mol-1
反应Ⅱ:2C(s)+O2(g)=2CO(g)△H2=-221kJ•mol-1
反应Ⅲ:N2(g)+O2(g)=2NO(g)△H3=+180.5kJ•mol-1
试回答下列问题:
(1)汽车尾气净化原理为反应Ⅳ:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-746.5 kJ•mol-1,该反应能自发进行的条件是低温.(填“高温”、“低温”或“任意温度”).
(2)如果在一定温度下,体积为 2 升的密闭容器中发生化学反应Ⅳ,0~4min各物质物质的量的变化如下表所示:
①求 0~2min 内用 CO 来表示的平均反应速率 v(CO)=0.10mol•Lˉ1•minˉ1.
②试计算该温度下反应Ⅳ的化学平衡常数 K=1.6.
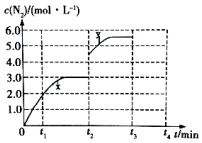
(3)若一定温度下,在容积可变的密闭容器中,上述反应Ⅳ达到平衡状态,此时容积为3L,c(N2)随时间 t 的变化曲线 x 如图所示.
①若在 t2min时改变一个条件,c(N2)随反应时间 t 的变化如曲线 y 所示,则改变的条件是快速将容器体积由3L压缩到2L.
②若在t2min时升高温度,t3min时重新达到平衡,请在图中画出在 t2~t4内 c(N2)的变化曲线.
 已知在298K和101kPa条件下,有如下反应:
已知在298K和101kPa条件下,有如下反应:反应Ⅰ:C(s)+O2(g)=CO2(g)△H1=-393.5kJ•mol-1
反应Ⅱ:2C(s)+O2(g)=2CO(g)△H2=-221kJ•mol-1
反应Ⅲ:N2(g)+O2(g)=2NO(g)△H3=+180.5kJ•mol-1
试回答下列问题:
(1)汽车尾气净化原理为反应Ⅳ:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-746.5 kJ•mol-1,该反应能自发进行的条件是低温.(填“高温”、“低温”或“任意温度”).
(2)如果在一定温度下,体积为 2 升的密闭容器中发生化学反应Ⅳ,0~4min各物质物质的量的变化如下表所示:
| 物质(mol) 时间 | NO | CO | N2 | CO2 |
| 起始 | 0.40 | 1.0 | ||
| 2min 末 | 2.0 | 0.80 | 1.6 | |
| 4min 末 | 1.6 |
②试计算该温度下反应Ⅳ的化学平衡常数 K=1.6.
(3)若一定温度下,在容积可变的密闭容器中,上述反应Ⅳ达到平衡状态,此时容积为3L,c(N2)随时间 t 的变化曲线 x 如图所示.
①若在 t2min时改变一个条件,c(N2)随反应时间 t 的变化如曲线 y 所示,则改变的条件是快速将容器体积由3L压缩到2L.
②若在t2min时升高温度,t3min时重新达到平衡,请在图中画出在 t2~t4内 c(N2)的变化曲线.
16.金属铁用途广泛,高炉炼铁的总反应为:Fe2O3 (s)+3CO(g)?2Fe(s)+3CO2(g),请回答下列问题:
(1)已知:
3Fe2O3 (s)+CO(g)?2Fe3O4(s)+CO2(g),△H=-47kJ/mol
Fe3O4 (s)+CO(g)?3FeO(s)+CO2(g),△H=-19kJ/mol
Fe3O4 (s)+CO(g)?Fe(s)+CO2(g),△H=-11kJ/mol
则Fe2O3 (s)+3CO(g)?2Fe(s)+3CO2(g)的)△H=-77kJ/mol.
(2)一定温度下,上述反应的化学平衡常数为8.0,该温度下将2molCO、2molFe2O3、6molCO2、5molFe加入容积为2L的密闭容器中,此时反应将向正反应方向进行(填“正”或“逆”或“处于平衡状态”),平衡时CO2的浓度为3.55mol/L;反应达平衡后,若升高温度,平衡常数K将减小(填“增大”“减小”“不变”).
(3)为使反应速率加快,且使反应产率增大,以下条件可行的是C
A.升高温度B.增加三氧化铁的质量C.催化剂+稍低温度
D.用氢氧化钠溶液吸收二氧化碳E.体积收缩增大压强 F.体积恒定增加N2
(4)上述总反应在高炉中大致分为三个阶段,各阶段主要成分与温度有关系如下表:
800℃时固体物质的主要成分为Fe3O4、FeO,该温度下若测得固体混合物中m(Fe):m(O)=105:32,Fe3O4被CO还原为FeO的百分率为85.7%(设其它固体杂质中不含Fe、O元素).
(1)已知:
3Fe2O3 (s)+CO(g)?2Fe3O4(s)+CO2(g),△H=-47kJ/mol
Fe3O4 (s)+CO(g)?3FeO(s)+CO2(g),△H=-19kJ/mol
Fe3O4 (s)+CO(g)?Fe(s)+CO2(g),△H=-11kJ/mol
则Fe2O3 (s)+3CO(g)?2Fe(s)+3CO2(g)的)△H=-77kJ/mol.
(2)一定温度下,上述反应的化学平衡常数为8.0,该温度下将2molCO、2molFe2O3、6molCO2、5molFe加入容积为2L的密闭容器中,此时反应将向正反应方向进行(填“正”或“逆”或“处于平衡状态”),平衡时CO2的浓度为3.55mol/L;反应达平衡后,若升高温度,平衡常数K将减小(填“增大”“减小”“不变”).
(3)为使反应速率加快,且使反应产率增大,以下条件可行的是C
A.升高温度B.增加三氧化铁的质量C.催化剂+稍低温度
D.用氢氧化钠溶液吸收二氧化碳E.体积收缩增大压强 F.体积恒定增加N2
(4)上述总反应在高炉中大致分为三个阶段,各阶段主要成分与温度有关系如下表:
| 温度 | 250℃600℃1000℃2000℃ |
| 主要成分 | Fe2O3 Fe3O4 FeO Fe |
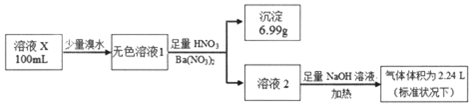
13.已知还原性:SO32->I-.某溶液X可能含有NH4+、Na+、Ba2+、Fe3+、I-、SO32-、SO42-中的几种,为确定其组成,某同学进行如图实验:下列说法正确的是( )
0 162561 162569 162575 162579 162585 162587 162591 162597 162599 162605 162611 162615 162617 162621 162627 162629 162635 162639 162641 162645 162647 162651 162653 162655 162656 162657 162659 162660 162661 162663 162665 162669 162671 162675 162677 162681 162687 162689 162695 162699 162701 162705 162711 162717 162719 162725 162729 162731 162737 162741 162747 162755 203614

| A. | 溶液X肯定只存在NH4+、SO42- | |
| B. | 溶液X一定不含有Ba2+、Fe3+,可能含有I- | |
| C. | 为确定可能存在的阴离子,可另取试液滴加足量盐酸、BaCl2溶液 | |
| D. | 为确定可能存在的阳离子,可用经过稀硫酸洗过的铂丝蘸取溶液X在酒精灯火焰上灼烧 |
 某红色固体粉末样品可能含有Fe2O3和Cu2O中的一种或两种,某化学兴趣小组对其组成进行探究.完成下列空格.
某红色固体粉末样品可能含有Fe2O3和Cu2O中的一种或两种,某化学兴趣小组对其组成进行探究.完成下列空格.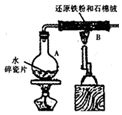 某校化学小组学生利用如图所示装置进行“铁与水反应”的实验,并探究固体产物成分(图中夹持及尾气处理装置均已略去).
某校化学小组学生利用如图所示装置进行“铁与水反应”的实验,并探究固体产物成分(图中夹持及尾气处理装置均已略去).