6.用沉淀法测定 KHCO3和 Na2CO3 固体混合物的组成,每次称取一定质量的样品溶于水制成溶液,向其中滴加相同浓度的 Ba(OH)2 溶液,每次实验均充分反应,反应前后溶液体积变化忽略不计,实验记录见表:
回答下列问题:
(1)样品中KHCO3和Na2CO3 的物质的量之比2:1.
(2)室温下第III组实验所得溶液中的 OH-物质的量浓度为0.6mol/L.
| 实验序号 | I | II | III | IV | Ⅴ |
| 样品质量(g) | 3.06 | 6.12 | 9.18 | 12.24 | 15.30 |
| Ba(OH)2溶液体积(mL) | 300 | 300 | 300 | 300 | 300 |
| 生成沉淀的质量(g) | 5.91 | 11.82 | 17.73 | 23.64 | 23.64 |
(1)样品中KHCO3和Na2CO3 的物质的量之比2:1.
(2)室温下第III组实验所得溶液中的 OH-物质的量浓度为0.6mol/L.
5.在下列反应中,水只作氧化剂的是( )
| A. | 2F2+2H2O═4HF+O2 | B. | 2Na+2H2O═2NaOH+H2↑ | ||
| C. | CaO+H2O═Ca(OH)2 | D. | 2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ |
4.某同学进行了硫代硫酸钠与硫酸反应的有关实验,实验过程的数据记录如表(见表格),请结合表中信息,回答有关问题:( Na2S2O3+H2SO4═Na2SO4+S↓+SO2↑+H2O)
(1)根据你所掌握的知识判断,在上述实验中,反应速率最快的可能是D(填实验序号).
(2)在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有关的各项反应条件,其中:
①能说明温度对该反应速率影响的组合是BD(填实验序号,下同);
②A和B、A和C的组合比较,所研究的问题是相同温度条件下浓度对该反应速率的影响;
③B和C的组合比较,所研究的问题是相同温度条件下,该反应速率更大程度上取决于哪种反应物的浓度
(3)教材中利用了出现黄色沉淀的快慢来比较反应速率的快慢,请你分析为何不采用排水法测量单位时间内气体体积的大小进行比较:SO2可溶于水,测定不精确或实验装置较复杂,不易控制.
| 实验 序号 | 反应温 度/℃ | 参加反应的物质 | ||||
| Na2S2O3 | H2SO4 | H2O | ||||
| V/mL | c/mol•L-1 | V/mL | c/mol•L-1 | V/mL | ||
| A | 20 | 10 | 0.1 | 10 | 0.1 | 0 |
| B | 20 | 5 | 0.1 | 10 | 0.1 | 5 |
| C | 20 | 10 | 0.1 | 5 | 0.1 | 5 |
| D | 40 | 5 | 0.1 | 10 | 0.1 | 5 |
(2)在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有关的各项反应条件,其中:
①能说明温度对该反应速率影响的组合是BD(填实验序号,下同);
②A和B、A和C的组合比较,所研究的问题是相同温度条件下浓度对该反应速率的影响;
③B和C的组合比较,所研究的问题是相同温度条件下,该反应速率更大程度上取决于哪种反应物的浓度
(3)教材中利用了出现黄色沉淀的快慢来比较反应速率的快慢,请你分析为何不采用排水法测量单位时间内气体体积的大小进行比较:SO2可溶于水,测定不精确或实验装置较复杂,不易控制.
3.在10℃和2×105 Pa的条件下,反应aA(g)?dD(g)+eE(g)建立平衡后,再逐步增大体系的压强(温度不变).表列出了不同压强下平衡时物质D的浓度.
根据表中数据,回答下列问题:
(1)压强从2×105 Pa增加到5×105 Pa时,平衡移动方向是左,理由是D浓度增大的倍数小于压强增大的倍数.
(2)压强从5×105 Pa增加到1×106 Pa时,平衡移动方向是右,理由是D浓度增大的倍数大于压强增大的倍数,此时压强增大可能使E液化,使生成物的气体体积减小.
| 压强(Pa) | 2×105 | 5×105 | 1×106 |
| 浓度(mol•L-1) | 0.085 | 0.20 | 0.44 |
(1)压强从2×105 Pa增加到5×105 Pa时,平衡移动方向是左,理由是D浓度增大的倍数小于压强增大的倍数.
(2)压强从5×105 Pa增加到1×106 Pa时,平衡移动方向是右,理由是D浓度增大的倍数大于压强增大的倍数,此时压强增大可能使E液化,使生成物的气体体积减小.
2.短周期元素的性质或原子结构如表:
(1)写出元素X的离子结构示意图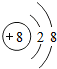 .写出元素Z的气态氢化物的电子式
.写出元素Z的气态氢化物的电子式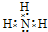 (用元素符号表示)
(用元素符号表示)
(2)写出Y元素最高价氧化物水化物的电离方程式H++AlO2-+H2O?Al(OH)3?Al3++3OH-.
(3)元素T与氯元素相比,非金属性较强的是F(用元素符号表示).
| 元素编号 | 元素性质或原子结构 |
| T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| X | L层p电子数比s电子数多2个 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | L层有三个未成对电子 |
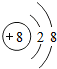 .写出元素Z的气态氢化物的电子式
.写出元素Z的气态氢化物的电子式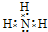 (用元素符号表示)
(用元素符号表示)(2)写出Y元素最高价氧化物水化物的电离方程式H++AlO2-+H2O?Al(OH)3?Al3++3OH-.
(3)元素T与氯元素相比,非金属性较强的是F(用元素符号表示).
1.设NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1.00mol NaCl中含有NA个NaCl 分子 | |
| B. | 常温常压下,22.4LCl2与足量镁粉反应,转移的电子数为2NA | |
| C. | 一定条件下,2.3gNa与足量O2完全反应生成3.6g产物时失去的电子数为0.1NA | |
| D. | 28g乙烯和环丙烷(C3H6)组成的混合气体中含有氢原子的个数为3 NA |
18.某研究小组利用图装置探究CO还原Fe2O3所得到的一种黑色粉末的成分(固定装置略去).(已知:Fe2+遇到K3溶液生成蓝色沉淀)

请回答问題:
(1)按气流方向,各仪器接口从左到右的连接顺序为:
i→c→d→g→h→a→b→j→k→f→e.(填字母编号)
(2)证明Fe2O3己被还原的现象是F中的固体由红棕色变黑色,C中溶液变浑浊.
(3)研究小组对黑色粉末的成分提出下列猜想:
【猜想一】黑色粉末的成分可能是Fe.
【猜想二】黑色粉末的成分可能是FeO.
【猜想三】黑色粉末的成分可能是Fe3O4.
设计并完成实验如表:
①根据实验现象,则猜想三成立.
②研究小组又向步骤3的溶液中滴加新制氯水,发现溶液红色褪去.可能的原因及验证方法为假设SCN-被Cl2氧化,向溶液中加入KSCN溶液,若出现红色,则假设成立.
(4)上述装置还有不妥之处,改进措施为在整套装置的尾气出口处,放置一燃着的酒精灯(或用导管将尾气引至F处酒精灯点燃).

请回答问題:
(1)按气流方向,各仪器接口从左到右的连接顺序为:
i→c→d→g→h→a→b→j→k→f→e.(填字母编号)
(2)证明Fe2O3己被还原的现象是F中的固体由红棕色变黑色,C中溶液变浑浊.
(3)研究小组对黑色粉末的成分提出下列猜想:
【猜想一】黑色粉末的成分可能是Fe.
【猜想二】黑色粉末的成分可能是FeO.
【猜想三】黑色粉末的成分可能是Fe3O4.
设计并完成实验如表:
| 步骤 | 操作 | 现象 |
| 1 | 加入稀盐酸 | 溶解,无气泡 |
| 2 | 取步骤1中溶液,滴加K3[Fe(CN)6]溶液 | 蓝色沉淀 |
| 3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 |
②研究小组又向步骤3的溶液中滴加新制氯水,发现溶液红色褪去.可能的原因及验证方法为假设SCN-被Cl2氧化,向溶液中加入KSCN溶液,若出现红色,则假设成立.
(4)上述装置还有不妥之处,改进措施为在整套装置的尾气出口处,放置一燃着的酒精灯(或用导管将尾气引至F处酒精灯点燃).
17.将等物质的量的X、Y气体充入一个容积可变的密闭容器中,在一定条件下发生如下反应并达到平衡:X(g)+Y(g)?3Z(g)△H<0.当改变某个条件并维持新条件直至达到新平衡,表中关于新平衡与原平衡的比较,正确的是( )
0 162542 162550 162556 162560 162566 162568 162572 162578 162580 162586 162592 162596 162598 162602 162608 162610 162616 162620 162622 162626 162628 162632 162634 162636 162637 162638 162640 162641 162642 162644 162646 162650 162652 162656 162658 162662 162668 162670 162676 162680 162682 162686 162692 162698 162700 162706 162710 162712 162718 162722 162728 162736 203614
| 选择 | 改变的条件 | 正、逆反应速率变化 | 新平衡和原平衡比较 |
| A | 增大压强 | 正、逆反应速率都增大量 | Z的浓度减小 |
| B | 充入少量Z | 逆反应速率增大 | X的体积分数不变 |
| C | 充入少量Z | v(逆)>v(正) | Z的浓度减小 |
| D | 升高温度 | 逆反应速率增大量大于 正反应速率增大量 | Z的体积分数变大 |
| A. | A | B. | B | C. | C | D. | D |
 NaCl
NaCl .
.