5.根据表信息回答以下问题:
部分短周期元素的原子半径及主要化合价
(1)E、F、G三元素形成的化合物中化学键类型是离子键和共价键.
(2)B、H两元素的最高价氧化物所对应的水化物相互反应的离子方程式是Al(OH)3+3H+═Al3++3H2O.
(3)实验室中制取H单质反应的化学方程式是MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
部分短周期元素的原子半径及主要化合价
| 元素 | A | B | C | D | E | F | G | H |
| 原子半 径(nm) | 0.130 | 0.118 | 0.090 | 0.102 | 0.073 | 0.154 | 0.037 | 0.099 |
| 主要 化合价 | +2 | +3 | +2 | +6,-2 | -2 | +1 | +1 | +7,-1 |
(2)B、H两元素的最高价氧化物所对应的水化物相互反应的离子方程式是Al(OH)3+3H+═Al3++3H2O.
(3)实验室中制取H单质反应的化学方程式是MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
4.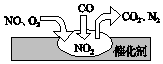 随着我国汽车年销量的大幅增加,空气环境受到了很大的污染.汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示,下列说法正确的是( )
随着我国汽车年销量的大幅增加,空气环境受到了很大的污染.汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示,下列说法正确的是( )
 随着我国汽车年销量的大幅增加,空气环境受到了很大的污染.汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示,下列说法正确的是( )
随着我国汽车年销量的大幅增加,空气环境受到了很大的污染.汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示,下列说法正确的是( )| A. | 反应中NO为氧化剂,N2为氧化产物 | |
| B. | 汽车尾气的主要污染成分包括CO、NO和N2 | |
| C. | NO和O2必须在催化剂表面才能反应 | |
| D. | 催化转化总化学方程式为2NO+O2+4CO=4CO2+N2 |
3.将容积为40mL的量筒充满二氧化氮和氧气的混合气体,将量筒倒置在盛满水的水槽里,一段时间后,量筒里剩余气体体积为5mL.则原混合气体中NO2和O2体积比可能是( )
| A. | 3:7 | B. | 7:1 | C. | 5:3 | D. | 1:1 |
2.下列叙述不正确的是( )
| A. | 钾、钠、镁等活泼金属着火时,不能用泡沫灭火器灭火 | |
| B. | 探究温度对硫代硫酸钠与硫酸反应速率的影响时,若先将两种溶液混合并计时,再用水浴加热至设定温度,则测得的反应速率偏低 | |
| C. | 滴定达终点时,发现滴定管尖嘴部分有悬滴,则测定结果偏小 | |
| D. | 为准确配制一定物质的量浓度的溶液,定容过程中向容量瓶内加蒸馏水至接近刻度线时,改用滴管滴加蒸馏水至刻度线 |
1.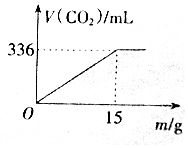 一定质量的铁碳合金在足量的氧气中燃烧,合金质量与生存二氧化碳体积(已换算为标准状况)关系如图所示,则此铁碳合金是( )
一定质量的铁碳合金在足量的氧气中燃烧,合金质量与生存二氧化碳体积(已换算为标准状况)关系如图所示,则此铁碳合金是( )
 一定质量的铁碳合金在足量的氧气中燃烧,合金质量与生存二氧化碳体积(已换算为标准状况)关系如图所示,则此铁碳合金是( )
一定质量的铁碳合金在足量的氧气中燃烧,合金质量与生存二氧化碳体积(已换算为标准状况)关系如图所示,则此铁碳合金是( )| A. | 低碳钢 | B. | 中碳钢 | C. | 高碳钢 | D. | 合金钢 |
20.如图用石墨电极电解CuCl2溶液.下列分析正确的是( )
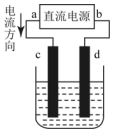

| A. | c极发生还原反应 | B. | 每生成6.4gCu,转移电子0.2mol | ||
| C. | 阳极反应式:Cu2++2e→Cu | D. | 在溶液中电子由d流向c |
17.将6.85g Fe和Al的混合物溶于200mL浓度为C mol/L的HNO3溶液中,得到标准状况下的NO、N2O混合气体共3.36L,测得反应后溶液的pH为0,再向所得溶液中加入过量NaOH溶液充分反应后生成沉淀质量为5.35g,若不考虑反应前后溶液体枳变化,则下列有关判断正确的是( )
0 162540 162548 162554 162558 162564 162566 162570 162576 162578 162584 162590 162594 162596 162600 162606 162608 162614 162618 162620 162624 162626 162630 162632 162634 162635 162636 162638 162639 162640 162642 162644 162648 162650 162654 162656 162660 162666 162668 162674 162678 162680 162684 162690 162696 162698 162704 162708 162710 162716 162720 162726 162734 203614
| A. | Fe与A1的物质的量之比为1:1 | |
| B. | 混合气体中 NO为0.03mol,N2O0.12mol | |
| C. | 原HNO3溶液的浓度C=4.6mol/L | |
| D. | 反应中被还原的HNO3为0.18 mol |
 .用电子式表示D2C的形成过程
.用电子式表示D2C的形成过程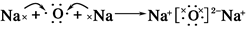 .
.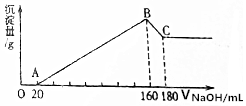 将一定质量的镁、铝合金,投入200mL一定浓度的盐酸中,合金完全溶解,向所得溶液中滴加5mol/L NaOH溶液,生成的沉淀质量与加入NaOH溶液体积如图所示.
将一定质量的镁、铝合金,投入200mL一定浓度的盐酸中,合金完全溶解,向所得溶液中滴加5mol/L NaOH溶液,生成的沉淀质量与加入NaOH溶液体积如图所示.