6.关于酸、碱、盐的下列各种说法中,正确的是( )
| A. | 化合物电离时,生成的阳离子有氢离子的是酸 | |
| B. | 化合物电离时,生成的阴离子有氢氧根离子的是碱 | |
| C. | 化合物电离时,生成金属阳离子和酸根离子的是盐 | |
| D. | NH4Cl通电时能电离出NH4+和Cl-,所以NH4Cl是盐 |
5.下列各物质中,第一种是酸、第二种是酸性氧化物、第三种是碱的是( )
| A. | 硫酸、干冰、纯碱 | B. | 硝酸、二氧化硫、苛性钠 | ||
| C. | 盐酸、氧化铜、熟石灰 | D. | 醋酸、水、烧碱 |
3. 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如表方案完成实验.
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如表方案完成实验.
(1)实验①和②的目的是探究浓度对反应速率的影响.
(2)写出实验③的化学反应方程式2H2O2$\frac{\underline{\;FeCl_{3}\;}}{\;}$O2↑+2H2O.
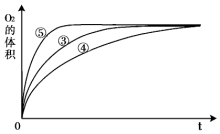
(3)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图.分析上图能够得出的实验结论是碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率.
 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如表方案完成实验.
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如表方案完成实验.| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol•L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol•L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol•L-1FeCl3溶液 |
(2)写出实验③的化学反应方程式2H2O2$\frac{\underline{\;FeCl_{3}\;}}{\;}$O2↑+2H2O.
(3)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图.分析上图能够得出的实验结论是碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率.
1.Na2SO3溶液做为吸收液吸收SO2时,吸收液pH随n(SO32-):n(HSO3-)变化的关系如表:
以下离子浓度关系的判断正确的是( )
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
| A. | Na2SO3溶液中c(H+)<c (OH-) | |
| B. | Na2SO3溶液中c(Na+))>c (SO32-)>c (HSO3-)>c (OH-)>c(H+) | |
| C. | 当吸收液呈中性时,c(Na+))>c (SO32-)>c (HSO3-)>c (OH-)=c(H+) | |
| D. | 当吸收液呈中性时,c(Na+)>c (HSO3-)+c (SO32-) |
20.下列曲线图(纵坐标为沉淀的物质的量,横坐标为加入物的量)不正确的是( )
| A. | 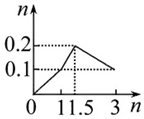 向1 L浓度均为0.1 mol•L-1的Ba(OH)2、NaAlO2混合液中加入0.1 mol•L-1稀硫酸 | |
| B. |  向1 L含有0.1 mol•L-1 AlCl3和0.3 mol•L-1 NH4Cl的混合液中加入0.1 mol•L-1 NaOH溶液 | |
| C. |  向烧碱溶液滴加明矾溶液 | |
| D. | 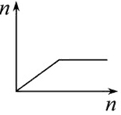 向AlCl3溶液滴加过量氨水 |
18.在同温、同压下,下列各组热化学方程式中,△H1>△H2的是( )
0 162525 162533 162539 162543 162549 162551 162555 162561 162563 162569 162575 162579 162581 162585 162591 162593 162599 162603 162605 162609 162611 162615 162617 162619 162620 162621 162623 162624 162625 162627 162629 162633 162635 162639 162641 162645 162651 162653 162659 162663 162665 162669 162675 162681 162683 162689 162693 162695 162701 162705 162711 162719 203614
| A. | 2H2(g)+O2(g)═2H2O(l)△H1 2H2(g)+O2(g)═2H2O(g)△H2 | |
| B. | S(g)+O2(g)═SO2 (g)△H1 S(s)+O2(g)═SO2 (g)△H2 | |
| C. | C(s)+O2(g)═CO(g)△H1 C(s)+O2(g)═CO2(g)△H2 | |
| D. | HCl(g)═H2(g)+Cl2(g)△H1 2HCl(g)═H2(g)+Cl2(g)△H2 |