17.化学与生产、生活密切相关,下列说法正确的是( )
| A. | 光导纤维导电能力很强,是一种很好的通讯材料 | |
| B. | 为了防止蛋白质盐析,疫苗等生物制剂应冷冻保藏 | |
| C. | 氯气泄漏时,应用浸有纯碱溶液的湿毛巾捂住口鼻向高处转移 | |
| D. | 用含有橙色酸性重铬酸钾的仪器检验酒后驾车,利用了乙醇的氧化性 |
14.中秋之夜,天宫二号搭载长征二号F运载火箭顺利升空,成为了中国第一个真正意义上的空间实验室.火箭使用的主要燃料是偏二甲肼(C2H8N2)和四氧化二氮,在火箭发射时反应的热化学方程式为:C2H8N2(l)+2N2O4(l)═2CO2(g)+3N2(g)+4H2O(g)△H=-2550kJ/mol,下列叙述错误的是( )
| A. | 该反应可在瞬间产生大量高温气体,推动火箭飞行且反应产物对环境无污染 | |
| B. | 向火箭注入燃料的操作非常严格,不能有丝毫失误,因为该反应的缺点是反应物有毒、有污染 | |
| C. | 偏二甲肼的燃烧热为△H=-2550 kJ/mol | |
| D. | 该反应中1mol C2H8N2反应时转移16 mol e- |
13. 中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%.
中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%.
(1)有效减碳的手段之一是节能,下列制氢方法最节能的是C.
A.电解水制氢:2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑
B.高温使水分解制氢:2H2O$\frac{\underline{\;高温\;}}{\;}$2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O$\frac{\underline{\;\;\;TiO_{2}\;\;\;}}{太阳光}$2H2↑+O2↑
D.天然气制氢:CH4+H2O$\frac{\underline{\;高温\;}}{\;}$CO+3H2
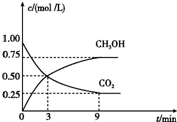
(2)CO2可转化成有机物实现碳循环.在体积为1L 的密闭容器中,充入1mol CO2和3mol H2,一定条件下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示.
①从3min到9min,v(H2)=0.125mol/(L•min).
②能说明上述反应达到平衡状态的是D(填编号).
A.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)工业上,CH3OH也可由CO和H2合成.参考合成反应CO(g)+2H2(g)?CH3OH(g)的平衡常数:
下列说法正确的是AC.
A.该反应正反应是放热反应
B.该反应在升高温度时,CH3OH(g)的体积分数减小,说明v正(CH3OH)减小,v逆(CH3OH)增大
C.在T℃时,1L密闭容器中,投入0.1mol CO和0.2mol H2,达到平衡时,CO转化率为50%,则此时的平衡常数为100
D.工业上采用稍高的压强(5Mpa)和250℃,是因为此条件下,原料气转化率最高.
 中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%.
中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%.(1)有效减碳的手段之一是节能,下列制氢方法最节能的是C.
A.电解水制氢:2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑
B.高温使水分解制氢:2H2O$\frac{\underline{\;高温\;}}{\;}$2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O$\frac{\underline{\;\;\;TiO_{2}\;\;\;}}{太阳光}$2H2↑+O2↑
D.天然气制氢:CH4+H2O$\frac{\underline{\;高温\;}}{\;}$CO+3H2
(2)CO2可转化成有机物实现碳循环.在体积为1L 的密闭容器中,充入1mol CO2和3mol H2,一定条件下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示.
①从3min到9min,v(H2)=0.125mol/(L•min).
②能说明上述反应达到平衡状态的是D(填编号).
A.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)工业上,CH3OH也可由CO和H2合成.参考合成反应CO(g)+2H2(g)?CH3OH(g)的平衡常数:
| 温度/℃ | 0 | 100 | 200 | 300 | 400 |
| 平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
A.该反应正反应是放热反应
B.该反应在升高温度时,CH3OH(g)的体积分数减小,说明v正(CH3OH)减小,v逆(CH3OH)增大
C.在T℃时,1L密闭容器中,投入0.1mol CO和0.2mol H2,达到平衡时,CO转化率为50%,则此时的平衡常数为100
D.工业上采用稍高的压强(5Mpa)和250℃,是因为此条件下,原料气转化率最高.
11.甲醛(CH2O)的水溶液叫做“福尔马林”,常用来保存动物标本.下列关于甲醛的叙述中,不正确的是( )
| A. | 一个甲醛分子由1个碳原子、2个氢原子、1个氧原子构成的 | |
| B. | 甲醛中碳、氢、氧三种元素的质量比为1:2:1 | |
| C. | 甲醛由碳、氢、氧三种元素组成的 | |
| D. | 甲醛中氧元素的质量分数为53.3% |
10.四种短周期元素在周期表中的相对位置如表格所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.
请回答下列问题:
(1)元素Z位于周期表中的位置第3周期第ⅤA族
(2)这些元素的氢化物中,水溶液碱性最强的是NH3(填写化学式,下同);X、Y、Z三种 元素的最高价氧化对应水化物中酸性由强到弱的依次为HNO3>H3PO4>H2CO3
(3)Y的气态氢化物和其最高价氧化物对应的水化物相互反应的离子方程式为:NH3+H+=NH4+.
0 162524 162532 162538 162542 162548 162550 162554 162560 162562 162568 162574 162578 162580 162584 162590 162592 162598 162602 162604 162608 162610 162614 162616 162618 162619 162620 162622 162623 162624 162626 162628 162632 162634 162638 162640 162644 162650 162652 162658 162662 162664 162668 162674 162680 162682 162688 162692 162694 162700 162704 162710 162718 203614
| X | Y | |
| Z | W |
(1)元素Z位于周期表中的位置第3周期第ⅤA族
(2)这些元素的氢化物中,水溶液碱性最强的是NH3(填写化学式,下同);X、Y、Z三种 元素的最高价氧化对应水化物中酸性由强到弱的依次为HNO3>H3PO4>H2CO3
(3)Y的气态氢化物和其最高价氧化物对应的水化物相互反应的离子方程式为:NH3+H+=NH4+.
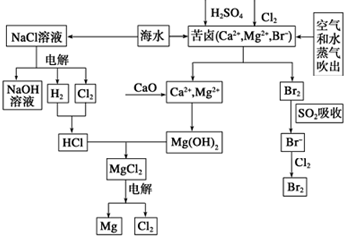 海水是宝贵的资源宝库,目前氯碱工业、海水提镁、海水提溴为人类提供了大量工业原料.下图是海水综合利用的部分流程图,据图回答问题:
海水是宝贵的资源宝库,目前氯碱工业、海水提镁、海水提溴为人类提供了大量工业原料.下图是海水综合利用的部分流程图,据图回答问题: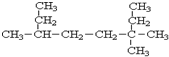 3,3,6-三甲基辛烷
3,3,6-三甲基辛烷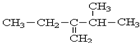 3-甲基-2-乙基-1-丁烯
3-甲基-2-乙基-1-丁烯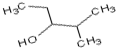 2-甲基-3-戊醇.
2-甲基-3-戊醇.