18.中华民族有着光辉灿烂的发明史,下列发明创造不涉及氧化还原反应的是( )
| A. | 用胆矾炼铜 | B. | 用铁矿石炼铁 | ||
| C. | 用黑火药开山炸石 | D. | 打磨磁石制指南针 |
17.某无色透明酸性溶液中,能大量共存的离子组是( )
| A. | Na+﹑Ca2+﹑Cl-﹑CO32- | B. | Na+、Ca2+、HCO3-、NO3- | ||
| C. | Cu2+﹑Cl-﹑Ca2+﹑NO3- | D. | NO3-﹑Na+﹑Ca2+﹑Cl- |
16.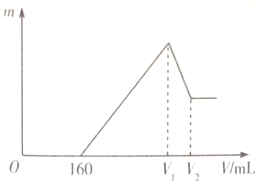 将0.1mol的Mg、Al混合物溶于100mL2mo L•L-1稀硫酸中,然后再滴加1moL•L-1 NaOH溶液.若在滴加NaOH溶液的过程中,沉淀质量(随加入NaOH溶液的体积(V)变化如图所示,当开始出现沉淀(不考虑混合时溶液体积的变化)下列判断正确的是( )
将0.1mol的Mg、Al混合物溶于100mL2mo L•L-1稀硫酸中,然后再滴加1moL•L-1 NaOH溶液.若在滴加NaOH溶液的过程中,沉淀质量(随加入NaOH溶液的体积(V)变化如图所示,当开始出现沉淀(不考虑混合时溶液体积的变化)下列判断正确的是( )
 将0.1mol的Mg、Al混合物溶于100mL2mo L•L-1稀硫酸中,然后再滴加1moL•L-1 NaOH溶液.若在滴加NaOH溶液的过程中,沉淀质量(随加入NaOH溶液的体积(V)变化如图所示,当开始出现沉淀(不考虑混合时溶液体积的变化)下列判断正确的是( )
将0.1mol的Mg、Al混合物溶于100mL2mo L•L-1稀硫酸中,然后再滴加1moL•L-1 NaOH溶液.若在滴加NaOH溶液的过程中,沉淀质量(随加入NaOH溶液的体积(V)变化如图所示,当开始出现沉淀(不考虑混合时溶液体积的变化)下列判断正确的是( )| A. | Mg与Al的质量比为3:2 | B. | (V1-160):(V2-V1)=3:1 | ||
| C. | 沉淀质量m最大=3.48 g | D. | V1时:c(Na+)=$\frac{400}{100+{V}_{1}}$mol•L-1 |
15.二茂铁[(C5H5)2Fe]的发现是有机金属化合物研究中具有里程碑意义的事件,它开辟了有机金属化合物研究的新领域.已知二茂铁熔点是173℃(在100℃时开始升华),沸点是249℃,不溶于水,易溶于苯、乙醚等非极性溶剂.下列说法不正确的是( )
| A. | 二茂铁属于分子晶体 | |
| B. | 在二茂铁结构中,C5H5-与Fe2+之间形成的化学键类型是离子键 | |
| C. | 已知环戊二烯的结构式为: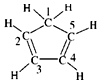 ,则其中仅有1个碳原子采取sp3杂化 ,则其中仅有1个碳原子采取sp3杂化 | |
| D. | C5H5-中一定含π键 |
13. 把一块镁铝合金投入到1mol/LHCl溶液里,待合金完全溶解后,往溶液里加入1mol/LNaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积的变化关系如图所示.下列说法中不正确的是( )
把一块镁铝合金投入到1mol/LHCl溶液里,待合金完全溶解后,往溶液里加入1mol/LNaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积的变化关系如图所示.下列说法中不正确的是( )
 把一块镁铝合金投入到1mol/LHCl溶液里,待合金完全溶解后,往溶液里加入1mol/LNaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积的变化关系如图所示.下列说法中不正确的是( )
把一块镁铝合金投入到1mol/LHCl溶液里,待合金完全溶解后,往溶液里加入1mol/LNaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积的变化关系如图所示.下列说法中不正确的是( )| A. | a的取值范围为0≤a<50 | |
| B. | 当a=30时,$\frac{n(Mg)}{n(Al)}$=1 | |
| C. | 图中0~a段,与NaOH发生反应的微粒是H+ | |
| D. | 当v(NaOH)=90mL时,溶液中的溶质为NaAlO2 |
11.为了测定K2CO3和NaHCO3混合物的组成,某学生每次称取一定质量的混合物溶于水配成溶液,向其中加入相同浓度的Ba(OH)2溶液,每次实验均充分反应,实验结果记录如下
请回答下列问题:
(1)第二次实验中产生沉淀的质量是2.758g;
(2)混合物中K2CO3和NaHCO3的物质的量之比为5:2.
| 实验次数 | 混合物的质量/g | 所加Ba(OH)2溶液的体积/L | 测得沉淀的质量/g |
| 1 | 0.858 | 0.5 | 1.379 |
| 2 | 1.716 | 0.5 | |
| 3 | 2.574 | 0.5 | 4.137 |
| 4 | 3.432 | 0.5 | 5.516 |
| 5 | 4.290 | 0.5 | 5.516 |
| 6 | 5.148 | 0.5 | 5.516 |
(1)第二次实验中产生沉淀的质量是2.758g;
(2)混合物中K2CO3和NaHCO3的物质的量之比为5:2.
10.把NaHCO3和Na2CO3•10H2O混合物5.38g溶于水制成100mL溶液,其中c(Na+)=0.4mol/L.如果把5.38g这种混合物加热至恒重所得固体的质量( )
0 162513 162521 162527 162531 162537 162539 162543 162549 162551 162557 162563 162567 162569 162573 162579 162581 162587 162591 162593 162597 162599 162603 162605 162607 162608 162609 162611 162612 162613 162615 162617 162621 162623 162627 162629 162633 162639 162641 162647 162651 162653 162657 162663 162669 162671 162677 162681 162683 162689 162693 162699 162707 203614
| A. | 2.65g | B. | 2.12g | C. | 3.9g | D. | 4.65g |
 将1.66g碳酸钠和氢氧化钠的固体混合物完全溶于水,配成稀溶液,然后向该溶液中逐滴加入1mo1•L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示.
将1.66g碳酸钠和氢氧化钠的固体混合物完全溶于水,配成稀溶液,然后向该溶液中逐滴加入1mo1•L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示.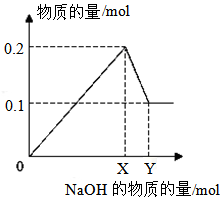 I.20mL0.1mol/LBaCl2溶液中Cl-的物质的量浓度为0.2mol/L,Ba2+的物质的量为0.002mol.
I.20mL0.1mol/LBaCl2溶液中Cl-的物质的量浓度为0.2mol/L,Ba2+的物质的量为0.002mol.