7.在C5H12的各种同分异构体中,所含甲基数目和它的一氯取代物的数目与叙述相符的是( )
| A. | 2个-CH3,能生成3种一氯代物 | B. | 3个-CH3,能生成3种一氯代物 | ||
| C. | 3个-CH3,能生成2种一氯代物 | D. | 4个-CH3,能生成2种一氯代物 |
4.等质量并且均过量的两份锌粉a和b(粉末表面积可视为相同,分别加入等体积等物质的量浓度的稀硫酸中,同时向a中加入少量硫酸铜,图表示产生H2的体积(V)与时间(t)的关系正确的是( )
| A. | 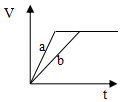 | B. | 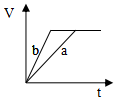 | C. | 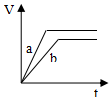 | D. | 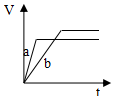 |
3.可逆反应:2NO2$\stackrel{△}{?}$2NO+O2在体积固定的密闭容器中,达到平衡状态的标志是:①单位时间内生成n molO2的同时生成2n molNO2②用NO2、NO、O2的物质的量浓度变化表示的反应速率比为2:2:1的状态③混合气体的颜
色不再改变的状态④混合气体的密度不再改变的状态⑤混合气体的平均摩尔质量不再改变的状态 ⑥混合气体的压强不再改变的状态( )
色不再改变的状态④混合气体的密度不再改变的状态⑤混合气体的平均摩尔质量不再改变的状态 ⑥混合气体的压强不再改变的状态( )
| A. | ①②③④ | B. | ③④⑤⑥ | C. | ①③⑤⑥ | D. | 全部 |
2.在一密闭容器中进行反应:2SO2(g)+O2(g)$?_{△}^{催化剂}$2SO3(g).已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.4mol/L、0.2mol/L、0.4mol/L.当反应达到平衡时,可能存在的数据是( )
| A. | SO2为0.8mol/L,O2为0.4 mol/L | B. | SO2为0.5 mol/L | ||
| C. | SO3为0.8 mol/L | D. | SO2、SO3均为0.3 mol/L |
1.某学生欲通过实验判断A、B、C三块金属的活动性,做了如下实验并得结论:当A与B组成原电池时,A 为电池的正极;当B与C组成原电池时,电流方向为由B到C,据此可知这三种金属的活动性强弱顺序为( )
| A. | A>B>C | B. | A>C>B | C. | C>B>A | D. | B>C>A |
20.下列变化中,未破坏化学键的是( )
| A. | HCl溶于水 | B. | 烧碱受热熔化 | C. | 碘的升华 | D. | CaO溶于水 |
19.下列关于如图所示原电池装置的叙述中,正确的是( )
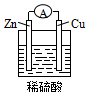

| A. | 铜片是负极 | B. | 氢离子在铜片表面被还原 | ||
| C. | 电流从锌片经导线流向铜片 | D. | 铜片质量逐渐减少 |
18.下列各元素的氧化物中,既能与盐酸反应生成盐和水,又能与NaOH溶液反应生成盐和水的是( )
0 162468 162476 162482 162486 162492 162494 162498 162504 162506 162512 162518 162522 162524 162528 162534 162536 162542 162546 162548 162552 162554 162558 162560 162562 162563 162564 162566 162567 162568 162570 162572 162576 162578 162582 162584 162588 162594 162596 162602 162606 162608 162612 162618 162624 162626 162632 162636 162638 162644 162648 162654 162662 203614
| A. | 元素X:位于元素周期表中的第三周期ⅢA 族 | |
| B. | 元素Y:它的二价阳离子核外电子总数与氖原子相同 | |
| C. | 元素Z:它的原子中M层比L层少2个电子 | |
| D. | 元素W:它的化合物的焰色反应颜色呈黄色 |
 某学习小组依据氧化还原反应:2Ag++Cu═Cu2++2Ag设计成的原电池如图所示,则负极发生的电极反应为Cu-2e-═Cu2+;当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移了的电子数目是0.05NA.
某学习小组依据氧化还原反应:2Ag++Cu═Cu2++2Ag设计成的原电池如图所示,则负极发生的电极反应为Cu-2e-═Cu2+;当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移了的电子数目是0.05NA.